题目内容
【题目】以氨气、空气为主要原料制硝酸。
(1)氨气被氧气催化氧化生成NO的化学方程式是______。
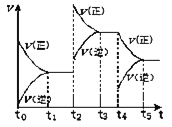
(2)在密闭容器中进行反应![]() 该反应的反应速率
该反应的反应速率![]() 随时间
随时间![]() 变化的关系如图所示,若
变化的关系如图所示,若![]() 、
、![]() 时刻只改变一个条件,下列说法正确的是
时刻只改变一个条件,下列说法正确的是![]() 填选项序号
填选项序号![]() ______。
______。
![]() 在
在![]() 时,可依据定容容器内气体的压强保持不变判断反应已达到平衡状态
时,可依据定容容器内气体的压强保持不变判断反应已达到平衡状态
![]() 在
在![]() 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度
![]() 在
在![]() 时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
![]() 在
在![]() 时,容器内
时,容器内![]() 的体积分数是整个过程中的最大值
的体积分数是整个过程中的最大值
【答案】![]() a
a
【解析】
(1)氨气被催化氧化生成NO和水,根据反应物和生成物及反应条件书写方程式;
(2)t2时,改变条件正逆反应速率都增大,且平衡正向移动,应该是增大压强;t4时,改变条件正反应速率不变、逆反应速率减小,平衡正向移动,改变的条件是减小生成物浓度;
a.恒温恒容时,该反应前后气体物质的量减小,则压强减小,可以根据压强是否改变平衡平衡状态;
b.在t2时,升高温度平衡逆向移动;
c.恒温恒容条件下,该反应前后气体总质量不变、容器体积不变,则密度始终不变;
d.t2时平衡正向移动、t4时减小二氧化氮浓度,平衡正向移动;
(1)氨气被催化氧化生成NO和水,根据反应物和生成物及反应条件书写方程式为![]() ,
,
故答案为:![]() ;
;
(2) t2时,改变条件正逆反应速率都增大,且平衡正向移动,应该是增大压强;![]() 时,改变条件正反应速率不变、逆反应速率减小,平衡正向移动,改变的条件是减小生成物浓度;
时,改变条件正反应速率不变、逆反应速率减小,平衡正向移动,改变的条件是减小生成物浓度;
![]() 恒温恒容时,该反应前后气体物质的量减小,则压强减小,当压强不变时该反应达到平衡状态,故a正确;
恒温恒容时,该反应前后气体物质的量减小,则压强减小,当压强不变时该反应达到平衡状态,故a正确;
![]() 在
在![]() 时,升高温度平衡逆向移动,与图象不符合,改变的条件是增大压强,故b错误;
时,升高温度平衡逆向移动,与图象不符合,改变的条件是增大压强,故b错误;
![]() 恒温恒容条件下,该反应前后气体总质量不变、容器体积不变,则密度始终不变,不能根据密度判断平衡状态,故c错误;
恒温恒容条件下,该反应前后气体总质量不变、容器体积不变,则密度始终不变,不能根据密度判断平衡状态,故c错误;
![]() 时平衡正向移动、
时平衡正向移动、![]() 时减小二氧化氮浓度,平衡正向移动,所以
时减小二氧化氮浓度,平衡正向移动,所以![]() 时二氧化氮体积分数最大,故d错误;
时二氧化氮体积分数最大,故d错误;
故答案选a。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】如图①、②、③、④、⑤五组仪器(可重复使用),选择合适的装置和药品能完成的实验是( )
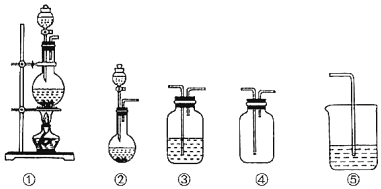
选项 | 实验目的 | 实验装置 | 实验药品 |
A | 制备并收集HCl气体 | ①③④ | 浓盐酸、浓硫酸、水 |
B | 比较氯气和溴的氧化性强弱 | ①③⑤ | MnO2、浓盐酸、饱和食盐水、溴化钾溶液、氢氧化钠溶液 |
C | 探究乙烯的加成反应 | ①③ | 无水乙醇、浓硫酸、溴的四氯化碳溶液 |
D | 探究二氧化硫的还原性 | ②③⑤ | 亚硫酸钠、30%的硝酸、溴水、氢氧化钠溶液 |
A.AB.BC.CD.D
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4