题目内容
【题目】中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池,如图所示,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料产生能量。下列说法正确的是( )
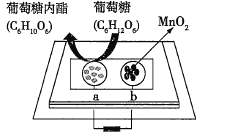
A.a极为正极
B.随着反应的进行,负极区的pH不断增大
C.消耗0.1mol葡萄糖,电路中转移0.2mol电子
D.b极的电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
【答案】C
【解析】
根据原电池装置图分析,葡萄糖(![]() )发生氧化反应生成葡糖糖内酯(
)发生氧化反应生成葡糖糖内酯(![]() ),则a极为负极,电极反应式为
),则a极为负极,电极反应式为 ,b极为正极,MnO2得到电子,发生还原反应,酸性条件下电极反应式为
,b极为正极,MnO2得到电子,发生还原反应,酸性条件下电极反应式为 ,据此结合选项分析可解答问题。
,据此结合选项分析可解答问题。
A.葡萄糖(![]() )发生氧化反应生成葡糖糖内酯(
)发生氧化反应生成葡糖糖内酯(![]() ),则a极为负极,A选项错误;
),则a极为负极,A选项错误;
B.根据负极电极反应,随着反应的进行,负极区的氢离子浓度逐渐增大,其溶液的![]() 不断减小,B选项错误;
不断减小,B选项错误;
C.由上述分析可知,负极的电极反应式为 ,消耗
,消耗![]() 葡萄糖,转移
葡萄糖,转移![]() 电子,C项正确;
电子,C项正确;
D.因电解质溶液呈酸性,则b极的电极反应式为 ,D选项错误;
,D选项错误;
答案选C。

练习册系列答案
相关题目
【题目】一定温度下,在3个容积均为![]() 的恒容密闭容器中反应
的恒容密闭容器中反应![]() 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
容器 | 温度 | 物质的起始浓度 | 物质的平衡浓度 | ||
|
|
|
| ||
Ⅰ | 400 |
|
| 0 |
|
Ⅱ | 400 |
|
| 0 |
|
Ⅲ | 500 |
|
| 0 |
|
A. 该反应的正反应是吸热反应
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C. 达到平衡时,容器Ⅱ中![]() 小于容器Ⅲ中
小于容器Ⅲ中![]()
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小