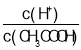题目内容
【题目】下列关系不正确的是( )
A.沸点:戊烷>2-甲基丁烷>2,2—二甲基丙烷>丙烷
B.密度:CCl4>CHCl3>H2O>苯
C.同分异构体数目:C5H12>C5H10>C4H10>C4H8>C3H8
D.等物质的量燃烧耗O2量:C5H12>C5H10>C4H10>C4H8>C3H8
【答案】C
【解析】
A.烷烃的碳原子数越多,沸点越高,相同碳原子数时支链越多沸点越低,沸点∶戊烷>2-甲基丁烷>2,2—二甲基丙烷>丙烷,故A正确;
B.相同碳原子数的氯代烃,含氯原子数越多密度越大,且大于水,苯的密度比水的密度小,则密度∶CCl4>CHCl3>H2O>苯,故B正确;
C.C5H12有正戊烷、异戊烷、新戊烷三种同分异构体,C4H10有正丁烷、异丁烷两种同分异构体,C3H8没有同分异构体,C5H10的烯烃同分异构体有5种,C4H8的烯烃同分异构体有3种,C5H10、C4H8除了烯烃同分异构体外还有环烷烃,故同分异构体数目∶C5H10>C4H8>C5H12>C4H10>C3H8,故C错误;
D.等物质的量的烃完全燃烧时,x+![]() (x为碳原子数,y为氢原子数)数值越大,燃烧耗O2量越多,则等物质的量燃烧耗O2量∶C5H12>C5H10>C4H10>C4H8>C3H8,故D正确;
(x为碳原子数,y为氢原子数)数值越大,燃烧耗O2量越多,则等物质的量燃烧耗O2量∶C5H12>C5H10>C4H10>C4H8>C3H8,故D正确;
答案选C。

【题目】(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g) |
| bB(g) |
| 2C(g) | |
起始物质的量浓度/(mol·L-1): | 1.5 | 1 | 0 | ||
2s末物质的量浓度/(mol·L-1): | 0.9 | 0.8 | 0.4 |
请回答下列问题。
①该可逆反应的化学方程式可表示为__。
②用物质B来表示0~2s的平均反应速率为__。
③从反应开始到2s末,A的转化率为__。
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是__(填序号)
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是__。
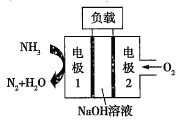
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为__;负极的电极反应式为__。