��Ŀ����
I. һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g����2H2��g��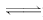 CH3OH��g����
CH3OH��g����
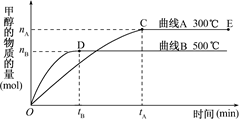
�������������ͼ��������и��⣺��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� ��
��2�������¶ȣ�Kֵ ���������С�����䡱����
II. ���淴Ӧ��aA��g��+ bB��g��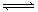 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�
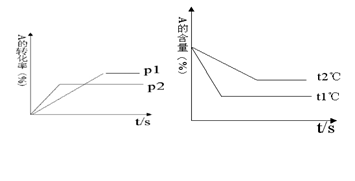
��1��ѹǿ P1��P2 ������С������2����a +b���ȣ�c +d�� ������С����
��3���¶�t1���t2�� �����ͣ�����4������ӦΪ ��Ӧ��
 CH3OH��g����
CH3OH��g����
�������������ͼ��������и��⣺��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� ��
��2�������¶ȣ�Kֵ ���������С�����䡱����
II. ���淴Ӧ��aA��g��+ bB��g��
 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�
��1��ѹǿ P1��P2 ������С������2����a +b���ȣ�c +d�� ������С����
��3���¶�t1���t2�� �����ͣ�����4������ӦΪ ��Ӧ��
I��1�� ����2����С II��1��С��2��С ��3���ߣ�4������
����2����С II��1��С��2��С ��3���ߣ�4������
 ����2����С II��1��С��2��С ��3���ߣ�4������
����2����С II��1��С��2��С ��3���ߣ�4���������������I.��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪ƽ�ⳣ������ʽK��
 ��
����2������ͼ���֪���¶�Խ�ߣ��״������ʵ���Խ�٣���˵�������¶�ƽ�����淴Ӧ�����ƶ������������¶�ƽ�ⳣ����С��
II��1��ѹǿΪP2ʱ���ȴﵽƽ��״̬������ѹǿ P1��P2С��
��2��ѹǿ�ߣ���Ӧ���ת���ʵͣ���˵������ѹǿƽ�����淴Ӧ�����ƶ�����������Ӧ���������Ŀ��淴Ӧ����a +b���ȣ�c +d��С��
��3���¶�Ϊt1ʱ���ȴﵽƽ��״̬�����¶�t1���t2��ߡ�
��4���¶ȸ߷�Ӧ���ת���ʵͣ���˵�������¶�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
�������������е��Ѷȵ����⣬���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ�����ȷ��Ӧ���ʺ�ƽ�ⳣ���ĺ����Լ�Ӱ�����أ�Ȼ������ͼ��ͷ���ʽ���������������ԭ���жϼ��ɡ�����������ѧ�������������������ѧ�����������ɡ��ܽ������������

��ϰ��ϵ�д�
�����Ŀ
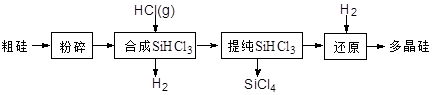
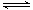 Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��
Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� �� H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
 2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ ��
2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ �� Z(g)����60 s�ﵽƽ�⣬����0.3 mol Z������˵����ȷ����( )
Z(g)����60 s�ﵽƽ�⣬����0.3 mol Z������˵����ȷ����( ) CH3CH2OH(g)+3H2O(g) ��
CH3CH2OH(g)+3H2O(g) ��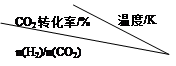
 2Z�� ��Ӧ�������еķ�Ӧ����(v)��ʱ��(t)�Ĺ�ϵ���ߣ�����������ȷ���� �� ��
2Z�� ��Ӧ�������еķ�Ӧ����(v)��ʱ��(t)�Ĺ�ϵ���ߣ�����������ȷ���� �� ��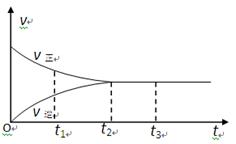
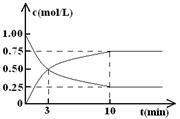
 C(��) ������ӦΪ���ȷ�Ӧ���ﵽƽ���������ͼ���жϣ�
C(��) ������ӦΪ���ȷ�Ӧ���ﵽƽ���������ͼ���жϣ�
 xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����O��8 mol B�������C��Ũ��ΪO��4 mol��L������д���пհף�
xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����O��8 mol B�������C��Ũ��ΪO��4 mol��L������д���пհף�