题目内容
【题目】下列有关物质的性质或用途的说法中正确的是
A. 氯气具有漂白性,可以使有色布条褪色
B. 二氧化硫具有较强的还原性,不能用浓硫酸干燥
C. SiO2是酸性氧化物,能与NaOH溶液反应
D. 氧化铁能与酸反应,可用于制作黑色颜料
【答案】C
【解析】A.氯气不具有漂白性,不能直接使有色布条褪色,必须是使湿润的有色布条褪色,具有漂白性的是次氯酸,故A错误;B.二氧化硫具有较强的还原性,但同种元素相邻价态间不发生氧化还原反应,所以能用浓硫酸干燥,故B错误;C.SiO2是酸性氧化物与碱反应生成盐和水,故C正确;D.氧化铁是难溶于水的红色固体,可以用做红色颜料,故D错误;故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】原电池是化学对人类的一项重大贡献。
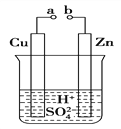
(1)某兴趣小组为研究原电池原理,设计如图A装置。
|
|
A | B |
①a和b不连接时,烧杯中发生反应的离子方程式是 _________________________。
②a和b用导线连接,Cu极为原电池________极(填“正”或“负”),该电极反应式是____________________。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子, 则理论上Zn片质量减轻________g。
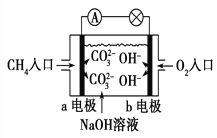
(2)如图是甲烷燃料电池原理示意图B,回答下列问题:
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: _________________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。