题目内容
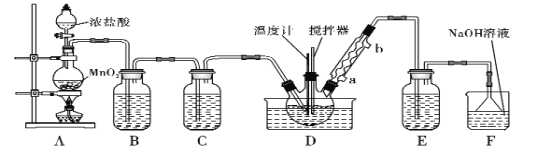
【题目】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质为黄绿色有毒气体。请回答下列问题:
(1)Q的离子结构示意图是__________________。
(2)六种元素中,原子半径最大的是___________。(写元素符号)
(3)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)____________。
(4)Y和Z的气态氢化物中,热稳定性强的是________(用物质化学式表示)。
(5)Y的气态氢化物与X和M形成的化合物反应,产物的化学式为________,其中存在的化学键类型为____________________。
(6)X与Z可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:_______________________________________________________________。
(7)单质M与水反应的离子方程式为____________________________________________。
【答案】 Na Cl->O2->Mg2+ H2O NH4Cl 离子键和共价键 2H2O2
Na Cl->O2->Mg2+ H2O NH4Cl 离子键和共价键 2H2O2![]() 2H2O+O2↑ Cl2+H2OH++Cl-+HClO
2H2O+O2↑ Cl2+H2OH++Cl-+HClO
【解析】
X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大.X是原子半径最小的元素,故X为H元素;Y的气态氢化物能使湿润的红色石蕊试纸变蓝,故为氨气,则Y为N元素;Z为地壳中含量最多的元素,故为O元素;R与X同主族,且原子序数大于8,故为Na元素;Y、R、Q最外层电子数之和为8,故Q的最外层有2个电子,且原子序数比11大,Q为Mg元素,M的单质黄绿色有害气体,故为Cl元素,据此分析结合元素性质解答。
(1) Q为Mg元素,镁原子核外有12个电子,失去两个电子变为镁离子,离子结构示意图是 ;
;
(2) X、Y、Z、R、Q、M是六种短周期元素,同周期元素随核电荷数增大,半径逐渐减小,同主族元素随核电荷数增大,半径逐渐增大,则短周期中原子半径最大的为Na元素;
(3) Z、Q、M简单离子分别为Cl-、O2-、Mg2+,而微粒的电子层数越多,则半径越大,故Cl的半径最大;当电子层数相同时,核电荷数越大,则半径越小,故Mg2+的半径最小,故简单离子半径由大到小的顺序为Cl->O2->Mg2+;
(4) Y为N元素,Z为O元素,其简单气态氢化物非别为NH3、H2O,非金属性越强,简单气态氢化物的稳定性越强,非金属性:O>N,则热稳定性强的是H2O。
(5) Y为N元素,气态氢化物为NH3,X为H元素,M为Cl元素,二者形成的化合物为HCl,二者反应生成氯化铵,产物的化学式为NH4Cl,为离子化合物,其中存在的化学键类型为离子键和共价键;
(6) Z为O元素,X为H元素,X与Z可分别形成10电子和18电子的分子分别为H2O和H2O2,H2O2在二氧化锰作催化剂条件下分解生成O2和H2O,化学方程式:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(7) M为Cl元素,氯气与水反应生成盐酸和次氯酸,为可逆反应,离子方程式为Cl2+H2OH++Cl-+HClO。

【题目】I.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
第二周期 | ① | ② | ③ | |||||
第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:________(填元素符号),
(2)在最高价氧化物对应的水化物中,碱性最强的化合物是________(填化学式),在常温下该化合物和元素⑦的单质反应的离子方程式__________。
(3)用电子式表示元素④与⑥的化合物的形成过程:__________。
(4)表示①与⑦的化合物的电子式_______,该化合物是由______(填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是____________(用化学式表示)。
II.①CBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He
只含有离子键的是(用序号回答)_____,即含离子键又含共价键是(用序号回答)_____,其中含有非极性共价键的共价化合物是(用序号回答)_____,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)_____。
【题目】有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A物质18.0g,升温使其汽化,测其密度是相同条 件下H2的45倍。 | A的相对分子质量为____ |
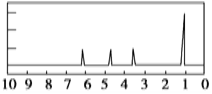
(2)A的核磁共振氢谱如下图:
| A中含有____种氢原子且吸收峰面积比为____ |
(3)另取A18.0g与足量的NaHCO3粉末反应,生成0.2mol CO2,若与足量钠反应则生成0.2molH2。 | A中所含官能团名称为______________ |
(4)将此18.0gA在足量O2中充分燃烧,并使其产物依次 缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8g和26.4g。 | A的分子式___________ |
(5)综上所述,A的结构简式为____ | |