题目内容
15.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )| A. | 化学反应速率关系是:3υ(NH3)═2υ(H2O) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 | |
| D. | 达到化学平衡时,5υ正(O2)=4υ逆(NO) |
分析 A、速率之比等于化学计量数之比;
B、都表示向反应正向进行,反应自始至终都是1:1,不能说明到达平衡;
C、增大体积压强减小,正逆速率都减小,平衡向体积增大的方向移动;
D、当反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆速率之比等于化学化学计量数之比(不同物质),各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化.
解答 解:A、反应处于平衡状态时,不同物质表示正逆反应速率之比等于化学计量数之比,应为3υ(NH3)═2υ(H2O),故A正确;
B、若单位时间内生成xmolNO的同时,消耗xmolNH3,都表示反应向正向进行,反应自始至终都是1:1,不能说明到达平衡,故B错误;
C、达到化学平衡时,若增加容器体积,则反应混合物的浓度减小,正、逆反应速率均减小,平衡向正反应移动,故C错误;
D、不同物质表示正逆反应速率之比等于化学计量数之比,4v正(O2)=5v逆(NO)表示反应达到平衡状态,5υ正(O2)=4υ逆(NO)的状态则不一定平衡,故D错误;
故选A.
点评 本题考查化学平衡状态的判断、平衡移动及影响平衡的因素等,题目难度中等,A选项中注意用不同物质的表示的正逆反应速率相等的表达方法,此为易错点.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
6.下列关于物质性质变化的比较,不正确的是( )
| A. | 酸性强弱:HIO4>HBrO4>HClO4 | B. | 原子半径大小:Na>Mg>Al | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
3.下列说法错误的是( )
| A. | 水玻璃可用于制备硅胶和木材防火剂 | |
| B. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| C. | 煤经过气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,PM2.5分散在空气中可能形成胶体或浊液 |
20.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16mol CO2和3.6g水,下列说法正确的是( )
| A. | 混合气体中一定有甲烷 | B. | 混合气体中一定是甲烷和乙烯 | ||
| C. | 混合气体中一定有乙烯 | D. | 混合气体中一定有乙炔 |
7.最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是( )
| A. | 该晶体类型是原子晶体 | |
| B. | 晶体的空间最小环共有6个原子构成 | |
| C. | 晶体中碳原子数与C-O化学键数之比为1:2 | |
| D. | 该晶体中碳原子和氧原子的个数比为1:2 |
4.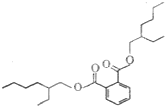 塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
 塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )| A. | 易溶于水,其水溶液有丁达尔效应 | B. | 在稀硫酸中不能稳定存在 | ||
| C. | 不能发生还原反应 | D. | 不能发生氧化反应 |
5.下列各组所有的元素组合,既可以构成离子晶体,又可以构成分子晶体的是( )
| A. | S.O.K | B. | Na.C.O | C. | H.O.S | D. | H.N.O |
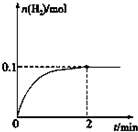 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应: