题目内容
下列叙述仪器“O”刻度位置正确的是( )
| A、在量筒的下端 |
| B、在普通温度计的中间 |
| C、在托盘天平标尺的正中 |
| D、在容量瓶的颈部 |
考点:计量仪器及使用方法
专题:化学实验常用仪器
分析:实验中的计量仪器都有一定的刻度,要了解常见刻度的变化情况:量筒从下而上的刻度是从小到大,它没有0刻度,温度计能够测量0上和0下温度,0刻度在中间,托盘天平游码标尺的刻度从左到右的刻度是从小到大,它的0刻度在左边,容量瓶是一种颈部细长的梨形瓶,只有最大容量一个刻度线,刻在瓶颈上,无0刻度.
解答:
解:A.量筒没有0刻度,量筒用于粗略量取液体体积,故A错误;
B.温度计0刻度在温度计的中间部分,故B正确;
C.托盘天平的0刻度在刻度尺的左端,故C错误;
D.容量瓶是一种颈部细长的梨形瓶,只有最大容量一个刻度线,刻在瓶颈上,无0刻度,故D错误;
故选B.
B.温度计0刻度在温度计的中间部分,故B正确;
C.托盘天平的0刻度在刻度尺的左端,故C错误;
D.容量瓶是一种颈部细长的梨形瓶,只有最大容量一个刻度线,刻在瓶颈上,无0刻度,故D错误;
故选B.
点评:本题考查了计量仪器的构造及使用方法,题目难度不大,注意掌握常见计量仪器的构造,实验中的计量仪器都有一定的刻度,要了解这些刻度的变化情况,如量筒是没有0刻度的,是易错点.

练习册系列答案
相关题目
下列有关金属的工业制法中,正确的是( )
| A、制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B、制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
| C、制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 |
| D、制铁:以铁矿石为原料,CO还原得铁 |
已知下列两个热化学方程式:
H2(g)+
O2(g)═H2O(l)△H=-285kJ?mol-1;C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2 220.0kJ?mol-1 实验测得H2和C3H8的混合气体共4mol,完全燃烧生成液态水时放热3075kJ,则混合气体中H2和C3H8的体积比是( )
H2(g)+
| 1 |
| 2 |
| A、1:2 | B、2:1 |
| C、3:1 | D、1:1 |
肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气.已知:N2(g)+2O2(g)═N2O4(g)△H=+8.7kJ/mol,N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是( )
| A、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-542.7kJ/mol |
| B、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1059.3kJ/mol |
| C、2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1076.7kJ/mol |
| D、N2H4(g)+N2O4(g)═N2(g)+2H2O(g)△H=-1076.7kJ/mol |
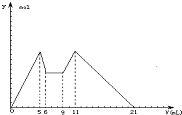 如图是向MgCl2和AlCl3混合液中,先加入NaOH溶液后又滴加盐酸,所得沉淀y(mol)与试剂体积V(mL)之间的关系.以下结论错误的是( )
如图是向MgCl2和AlCl3混合液中,先加入NaOH溶液后又滴加盐酸,所得沉淀y(mol)与试剂体积V(mL)之间的关系.以下结论错误的是( )| A、c(NaOH):c(HCl)=2:1 |
| B、原混合液中c(Al3+):c(Mg2+):c(Cl-)=1:1:5(不考虑离子的水解) |
| C、NaOH和盐酸的分界点是6mL处 |
| D、从7到9,都发生离子反应H++OH-→H2O |
在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)的平衡常数为K,下列说法正确的是( )
| A、增加A的量,平衡正向移动,达到新平衡时K值增大 | ||
| B、升高温度,K值增大 | ||
| C、K越大,说明该反应的进行程度越大,转化率越高 | ||
D、该反应的K=
|
化学与生活密切相关.下列生活中常见物质的俗名与化学式相对应的是( )
| A、苏打-NaHCO3 |
| B、胆矾-CuSO4 |
| C、酒精-CH3OH |
| D、生石灰-CaO |
关于3Cl2+6KOH═KClO3+5KCl+3H2O的反应,以下说法正确的是( )
| A、Cl2是氧化剂,KOH是还原剂 |
| B、被还原的氯元素的质量是被氧化的氯元素质量的5倍 |
| C、若反应中消耗12mol KOH,则转移10mol电子 |
| D、将KClO3和KCl的混合物加入到硫酸中反应,不可能产生Cl2 |