题目内容
12.工业上从海水中提取单质溴可采用如下方法:(1)向浓缩的海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为Cl2+2Br-=2Cl-+Br 2.
(2)向上述混合液中吹入热空气,将生成的溴蒸气吹出,用纯碱溶液吸收,其化学方程式为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2.
(3)将(2)所得溶液用H2SO4酸化,使NaBr,NaBrO3中的溴转化为单质溴,用有机溶剂通过萃取分离出粗溴,还可得到副产品Na2SO4.这一过程用到的化学方程式为5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br 2+3H2O.
(4)这样得到的粗溴中还混有少量的Cl2,除去的方法是加入NaBr,充分搅拌,再蒸馏得到纯净液溴.
分析 (1)氯气氧化性强于溴单质,氯气与溴离子反应生成溴单质和氯离子,据此写出反应的离子方程式;
(2)溴单质与纯碱溶液反应生成溴化钠、溴酸钠和二氧化碳气体,据此写出反应的化学方程式;
(3)依据溴单质在四氯化碳中的溶解度大,可以利用有机溶剂萃取溴单质,分离得到溴单质,将(2)所得溶液用H2SO4酸化,使NaBr,NaBrO3中的溴转化为单质溴和硫酸钠,该反应中溴元素化合价向中间靠拢,根据化合价升降法配平该方程式;
(4)根据氯气能够与溴化钠反应生成氯化钠和溴单质,可以除去杂质氯气,溴单质易挥发,加热蒸馏得到纯净液溴.
解答 解:(1)通入氯气后,氯气与溴离子反应生成单质溴和溴离子,其离子方程式为:Cl2+2Br-═2Cl-+Br2,
故答案为:Cl2+2Br-═2 Cl-+Br2;
(2)纯碱溶液吸收Br2的化学方程式为:3Na2CO3+3Br2=5NaBr+NaBrO3+3CO2↑,
故答案为:3Na2CO3+3Br2=5NaBr+NaBrO3+3CO2↑;
(3)将(2)所得溶液用H2SO4酸化,使NaBr,NaBrO3中的溴转化为单质溴和硫酸钠,溴酸根离子中溴元素化合价为+5价变成0价,化合价降低5价;溴离子化合价由-1价到0价,化合价升高1价,则化合价变化的最小公倍数为5,所以溴酸根离子计量数为1,溴离子计量数为5,再根据观察法配平,配平后反应的化学方程式为:5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br 2+3H2O
故答案为:萃取;5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br 2+3H2O;
(4)利用NaBr溶液与Cl2反应生成溴单质和氯离子,然后分液可除去Cl2,溴单质是易挥发的液体,通过蒸馏得到溴单质,
故答案为:NaBr;蒸馏.
点评 本题考查了氯、溴、碘及其化合物的性质,题目难度中等,试题涉及了离子方程式、化学方程式、氧化还原反应的配平等知识,注意掌握卤素单质化学性质及相互之间发生置换反应.

 阅读快车系列答案
阅读快车系列答案(1)用电弧法合成的储氢材料常伴有大量的碳纳米颗粒(杂质),这些杂质颗粒通常用硫酸酸化的锰酸钾氧化除去,在反应中,杂质碳被氧化为无污染气体而除去,Mn元素转变为Mn2+,请写出对应的化学方程式并配平:C+K2MnO4+2H2SO4=CO2↑+MnSO4+K2SO4+2H2O;
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?
CO2(g)+H2(g),得到如下两组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
②下列方法中可以证明上述已达平衡状态的是ae;
a.单位时间内生成n mol H2的同时生成n mol CO
b.容器内压强不再变化 c.混合气体密度不再变化
d.混合气体的平均相对分子质量不再变化 e.CO2的质量分数不再变化
③已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表,则反应CO(g)+H2O(g)?CO2(g)+H2(g),在900K时,该反应平衡常数的对数值(lgK)=0.36.
| 气化反应式 | lgK | ||
| 700K | 900K | 1200K | |
| C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
| C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
C(s)+O2(g)=CO2(g)△H 1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g)△H 2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g)△H 3=-296.0kJ•mol-1
请写出CO除SO2的热化学方程式2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1.
(4)25°C时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中c(CO32-)=0.2mol/L,如果加入等体积的Na2SO4溶液,若要产生 BaSO4沉淀,加入Na2SO4溶液的物质的量浓度最小是0.01mol/L.
(5)25℃时,在20mL0.1mol/L醋酸中加入V mL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是BC.

A.pH=3的CH3COOH溶液和pH=11的CH3COONa溶液中,由水电离出的c(OH-)相等
B.①点时pH=6,此时溶液中,c(CH3COO-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(CH3COO-)=c(Na+)
D.③点时V=20mL,此时溶液中c(CH3COO-)<c(Na+)=0.1mol/L
(6)如图是一种新型燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电进行粗铜的精炼实验.回答下列问题:
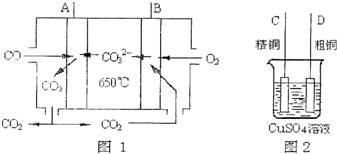
①写出A极发生的电极反应式CO-2e-+CO32-=2CO2 ;
②要用燃料电池为电进行粗铜的精炼实验,则B极应该与D极(填“C”或“D”)相连.
| A. | 等质量的N2和CO含有相同数目的原子 | |
| B. | 1mol臭氧和1.5mol氧气含有相同的氧原子数 | |
| C. | 1mol氧气中含有12.04×1023个氧原子,在常温常压下占有体积22.4L | |
| D. | 等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
| A. | 3种 | B. | 5种 | C. | 6种 | D. | 11种 |
 .
.

 为治理环境,减少雾霾,工业上通常用下列方法治理CO2和硫、氮氧化物的污染.
为治理环境,减少雾霾,工业上通常用下列方法治理CO2和硫、氮氧化物的污染.