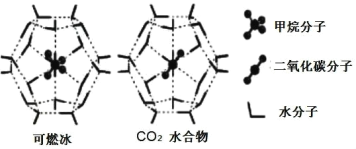
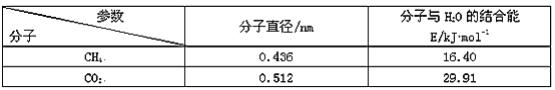
题目内容
【题目】氧气是一种清洁能源,氧气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=206.2 kJ![]()
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH=247.4 kJ![]()
2H2S(g)=2H2(g)+S2(g)ΔH=169.8 kJ![]()
以甲烷为原料制取氢气是工业上常用的制氢方法。CH4与 H2O(g)反应生成CO2(g)和 H2(g)的热化学方程式为_______。
【答案】CH4(g)+2H2O(g)=CO2(g)+4H2(g)ΔH=+165.0 kJ![]()
【解析】
已知:①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJmol-1;②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJmol-1,结合盖斯定律可知,①×2-②得到CH4(g)+2H2O(g)=CO2(g)+4H2(g),以此来解答。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=206.2 kJ![]() ,② CH4(g)+CO2(g)= 2CO(g)+2H2(g)ΔH=247.4 kJ
,② CH4(g)+CO2(g)= 2CO(g)+2H2(g)ΔH=247.4 kJ![]() ,结合盖斯定律可知,①×2-②得到CH4(g)+2H2O(g)=CO2(g)+4H2(g),△H=(+206.2kJmol-1)×2-(+247.4kJmol-1)=+165kJmol-1,则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165kJmol-1,。
,结合盖斯定律可知,①×2-②得到CH4(g)+2H2O(g)=CO2(g)+4H2(g),△H=(+206.2kJmol-1)×2-(+247.4kJmol-1)=+165kJmol-1,则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165kJmol-1,。

 阅读快车系列答案
阅读快车系列答案【题目】以氮化镓(GaN)、砷化镓(GaAs)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点,如砷化镓灯泡寿命是普通灯泡的100倍,而耗能即为10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。请回答下列问题:
(1)基态镓原子的价电子排布式为___。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为__和+3。砷的电负性比镓__(填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,GaCl3、GaBr3、GaI3的熔、沸点依次升高,分析其变化原因:__。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是__。
(4)①砷化镓是将(CH3)3Ga和AsH3用MOCVD(金属有机物化学气相淀积)方法制备得到的,该反应在700℃进行,反应的方程式为:___。
②反应物AsH3分子的几何构型为__,(CH3)3Ga中镓原子杂化方式为__。
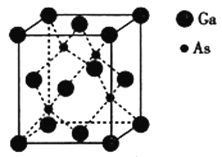
(5)砷化镓熔点为1238℃,立方晶胞结构如图所示,晶胞参数为a=565pm,As的配位数为__,晶体的密度为__(设NA为阿伏加德罗常数的数值,列出算式即可)g·cm-3。