题目内容
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—PakJ·mol-1、P—ObkJ·mol-1、P=OckJ·mol-1、O=OdkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热______。
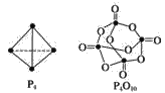
【答案】(6a+5d﹣4c﹣12b)kJ·mol-1
【解析】
热化学方程式的焓变△H=反应物总键能-生成物总键能,据此计算判断。
由题意,各化学键键能为P—PakJ·![]() 、P—ObkJ·
、P—ObkJ·![]() 、P=OckJ·
、P=OckJ·![]() 、O=OdkJ·
、O=OdkJ·![]() 。反应热ΔH=反应物总键能-生成物总键能,所以反应P4+5O2=P4O10的反应热△H=6akJ·
。反应热ΔH=反应物总键能-生成物总键能,所以反应P4+5O2=P4O10的反应热△H=6akJ·![]() +5dkJ·
+5dkJ·![]() -(4ckJ·
-(4ckJ·![]() +12bkJ·
+12bkJ·![]() )=(6a+5d﹣4c﹣12b)kJ·
)=(6a+5d﹣4c﹣12b)kJ·![]() ,
,
故答案为:(6a+5d﹣4c﹣12b)kJ·mol-1。

练习册系列答案
相关题目
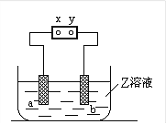
【题目】右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的
a电极 | b电极 | x电极 | Z溶液 | |
A | 铜 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A.AB.BC.CD.D