题目内容
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)O原子核外电子的运动状态有____种。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为____。
(3)下列关于CH4和CO2的说法正确的是____(填序号)。
a.固态CO2属于分子晶体,在晶体中一个CO2分子周围有12个紧邻的CO2分子
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(4)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2
①基态Ni原子的电子排布式为____,该元素位于元素周期表的第____周期____族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有____mol σ键。
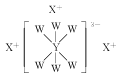
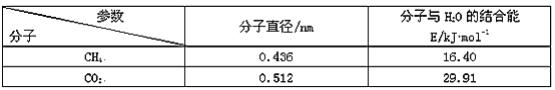
(5)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
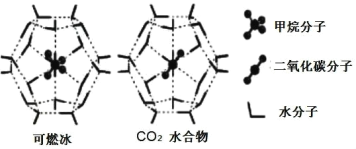
①“可燃冰”中分子间存在的2种作用力是____。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是____。
【答案】8 H、C、O a、d 1s22s22p63s23p63d84s2或[Ar]3d84s2 四 Ⅷ 8 氢键、范德华力 CO2的分子直径小于笼状结构空腔直径,且与H2O的结合能大于CH4
【解析】
(1)一个原子中不存在两个运动状态完全相同的电子, 所以有多少个电子,就有多少电子运动状态 ;
(2)元素的非金属性越强,其电负性越大;
(3)依据二氧化碳和甲烷的结构以及性质回答;
(4)①Ni为28号元素;
②该配合物的配离子中Ni原子和C原子、CO分子中C原子和O原子之间都存在σ键;
(5)①可燃冰中存在水分子,水分子中存在分子间作用力和氢键;
②依据表格得出二氧化碳的分子直径小于0.586nm,且与水的结合能力为29.91大于16.40,据此解答即可.
(1)O原子核外有8个电子,每个电子运动状态都不同,故答案为:8;
(2)电负性可以依据周期表判断, 同周期自左向右,非金属性增强即电负性增强;同族元素,自上而下非金属性减弱即电负性减小,故CH4和CO2所含的三种元素电负性从小到大的顺序为H、C、O;
(3)依据二氧化碳和甲烷的结构以及性质回答;
a.固态CO2属于分子晶体,由其晶胞结构可知,在晶体中一个CO2分子周围有12个紧邻的CO2分子,a正确;
b.CH4分子中含有极性共价键,但CH4正负电荷重心重合,是非极性分子,b错误;
c. CH4和CO2是分子晶体,不能根据键能比较它们的熔点,c错误;
d. CH4的C原子的价层电子对数为4,属于sp3杂化,CO2分子中碳原子的价层电子对数为2,杂化类型sp,d正确;
故选a、d;
(4)①Ni为28号元素,基态Ni原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,该元素位于元素周期表的第四周期第Ⅷ族;
②正四面体形的配合物Ni(CO)4中Ni原子和C原子、CO分子中C原子和O原子之间都存在σ键,故1mol Ni(CO)4中含有8mol σ键;
(5)①可燃冰中存在水分子,水分子中存在分子间作用力和氢键,“可燃冰”中分子间存在的2种作用力是氢键、范德华力;
②已知图中笼状结构的空腔直径为0.586nm,依据表格得出二氧化碳的分子直径小于0.586nm,且与水的结合能力为29.91大于16.40,故从物质结构及性质的角度分析,科学家用CO2置换CH4的设想的依据是CO2的分子直径小于笼状结构空腔直径,且与H2O的结合能大于CH4。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】下列①②对应的试剂(或条件)不能完成实验目的的是( )
![]()
实验目的 | 试剂(条件) | |
A | 温度对Na2S2O3溶液与H2SO4溶液反应速率的影响 | ①热水浴②冷水浴 |
B | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇②煤油 |
C | 用硝酸酸化的AgNO3溶液检验自来水中能否蒸馏除去Cl- | ①自来水②蒸馏水 |
D | 催化剂对H2O2分解速率的影响 | ①0.1mol/LFeCl3 ②0.2mol/LFeCl3 |
A.AB.BC.CD.D