题目内容
18.氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,该族元素的化合物在研究和生产中有许多重要用途.下列有关说法正确的( )| A. | H2O2、H2S、H2Se分子中均只含极性键 | |
| B. | 沸点:H2O<H2S<H2Se | |
| C. | 稳定性:H2O<H2S<H2Se | |
| D. | 上述元素的最高价氧化物对应的水化物中酸性最强的是H2SO4 |
分析 A、H2O2中含有氧-氧非极性共价键;
B、水分子间存在氢键;
C、非金属性越强氢化物越稳定;
D、元素非金属性越强,最高价氧化物对应水化物的酸性越强.
解答 解:A、H2O2中含有氧氧非极性共价键,而H2S、H2Se分子中均只含极性键,故A错误;
B、水分子间存在氢键,所以沸点:H2S<H2Se<H2O,故B错误;
C、非金属性越强氢化物越稳定,非金属性O>S>Se,所以氢化物的稳定性:H2O>H2S>H2Se,故C错误;
D、氧元素无正价,而非金属性:S>Se,所以酸性最强的是H2SO4,故D正确;
故选D.
点评 本题考查同一主族元素性质的递变规律与原子结构之间的关系,解决这类问题时学生要抓住特殊的物质,这是解这种题的关键,比如B选项中的水,比较容易.

练习册系列答案
相关题目
3.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,当①②相连时,外电路电流从②流向①;当①③相连时,溶液中的H+向③移动;当②④相连时,②上有气泡逸出;当③④相连时,③的质量减少.据此判断这四种金属活动性由大到小的顺序是( )
| A. | ①③②④ | B. | ③④②① | C. | ①③④② | D. | ③①②④ |
10.乙醇(CH3CH2OH)和二甲醚(CH3-O-CH3)互为( )的同分异构体.
| A. | 位置异构 | B. | 官能团异构 | C. | 手性异构 | D. | 碳链异构 |
7.下列有关电解质溶液的说法正确的是( )
| A. | Na2SO3溶液加水稀释后,pH和Kw均减小 | |
| B. | 0.1mol/L Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) | |
| C. | 浓度分别为0.2mol/L和0.1mol/L的CH3COOH溶液中,c(H+)之比小于2:1 | |
| D. | 室温下,pH=12的氨水与pH=2的H2SO4溶液等体积混合后,溶液呈酸性 |
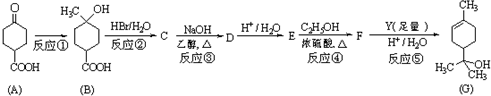
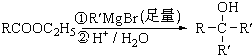
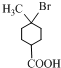 +2NaOH
+2NaOH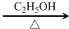
 +NaBr+2H2O.
+NaBr+2H2O.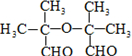 .
. H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下
H2(g)+CO2(g)△H﹤0,在其他条件不变的情况下 有机物A分子的结构简式为
有机物A分子的结构简式为 ;
; ;
; .
.