题目内容
3.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,当①②相连时,外电路电流从②流向①;当①③相连时,溶液中的H+向③移动;当②④相连时,②上有气泡逸出;当③④相连时,③的质量减少.据此判断这四种金属活动性由大到小的顺序是( )| A. | ①③②④ | B. | ③④②① | C. | ①③④② | D. | ③①②④ |
分析 ①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,组成的原电池中,较活泼的金属作负极、较不活泼的金属作正极,电流从正极沿导线流向负极;电解质溶液中阳离子向正极移动、阴离子向负极移动;负极上失电子发生氧化反应,正极上氢离子得电子发生还原反应,据此分析解答.
解答 解:①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,组成的原电池中,较活泼的金属作负极、较不活泼的金属作正极,电流从正极沿导线流向负极;电解质溶液中阳离子向正极移动、阴离子向负极移动;负极上失电子发生氧化反应,正极上氢离子得电子发生还原反应,
当①②相连时,外电路电流从②流向①,正极是②、负极是①,活动性①>②;
当①③相连时,溶液中的H+向③移动,正极是③、负极是①,活动性①>③;
当②④相连时,②上有气泡逸出,负极是④、正极是②,活动性④>②;
当③④相连时,③的质量减少,负极是③、正极是④,活动性③>④,
所以通过以上分析知,金属活动性强弱顺序是①③④②,
故选C.
点评 本题以原电池原理为载体考查金属活动性强弱顺序判断,侧重考查学生分析判断能力,明确原电池正负极与金属活动性强弱关系是解本题关键,还可以根据金属最高价氧化物的水化物碱性、金属之间的置换反应等判断金属性强弱,题目难度不大.

练习册系列答案
相关题目
16.向某无色溶液中加入铝片能放出氢气,则此溶液中一定能大量共存的离子组是( )
| A. | Ba2+、Cl-、Na+、K+ | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、SO32-、Cl-、NO3- | D. | Fe3+、Na+、AlO2-、SO42- |
14.某化学兴趣小组为提取海带中的碘,设计如图所示的流程,下列有关说法正确的是( )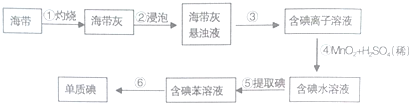

| A. | 步骤①④⑤均属于化学变化 | |
| B. | 步骤④中MnO2的作用是催化剂 | |
| C. | 步骤⑤所用主要仪器是分液漏斗、烧杯 | |
| D. | 步骤⑥操作名称是萃取、分液 |
11.有机化合物A的分子式为C5H12O,且能与金属钠反应放出氢气,那么A的同分异构体的数目(包括A)为( )
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
18.氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,该族元素的化合物在研究和生产中有许多重要用途.下列有关说法正确的( )
| A. | H2O2、H2S、H2Se分子中均只含极性键 | |
| B. | 沸点:H2O<H2S<H2Se | |
| C. | 稳定性:H2O<H2S<H2Se | |
| D. | 上述元素的最高价氧化物对应的水化物中酸性最强的是H2SO4 |
8.现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)B基态原子中能量最高的电子所处的能级为2p其电子云在空间有3个方向,原子轨道呈纺锤形;
(2)某同学根据上述信息,推断C基态原子的核外电子排布为,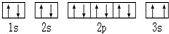 ,该同学所画的电子排布图违背了泡利不相容原理
,该同学所画的电子排布图违背了泡利不相容原理
(3)G位于ⅦB族d区,价电子排布式为3d54s2
(4)DE3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其空间构型为三角锥形
(5)1mol(SCN)2分子中含有σ键的数目为5NA;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键.
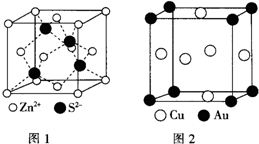
(6)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为4.
(7)铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密度为$\frac{389}{{N}_{A}×{a}^{3}×1{0}^{-21}}$(用含“a、NA 的代数式表示)g•cm-3.

| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 G在周期表的第七列 |
(2)某同学根据上述信息,推断C基态原子的核外电子排布为,
 ,该同学所画的电子排布图违背了泡利不相容原理
,该同学所画的电子排布图违背了泡利不相容原理(3)G位于ⅦB族d区,价电子排布式为3d54s2
(4)DE3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其空间构型为三角锥形
(5)1mol(SCN)2分子中含有σ键的数目为5NA;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键.
(6)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为4.
(7)铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密度为$\frac{389}{{N}_{A}×{a}^{3}×1{0}^{-21}}$(用含“a、NA 的代数式表示)g•cm-3.
15.下列各组物质中,化学键类型和化合物类型都相同的是( )
| A. | SO2和H2O | B. | CO2和Na2CO3 | C. | KOH和NaCl | D. | NaCl和HCl |
12.下列属于吸热反应的是( )
| A. | 液态水气化 | B. | 氢气燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl(s)混合 |
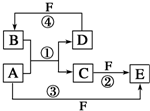 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出). ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.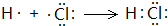 .
.