题目内容
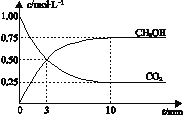
【题目】已知:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH =-49.0 kJmol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是 ( )
CH3OH(g) + H2O(g) ΔH =-49.0 kJmol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是 ( )
A. 升高温度能使![]() 增大
增大
B. 反应达到平衡状态时,CO2的平衡转化率为75%
C. 3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D. 从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 molL-1min-1
【答案】B
【解析】
从勒夏特列原理、化学反应速率计算的角度进行分析。
A、该反应为放热反应,升高温度,平衡向逆反应方向进行,CH3OH物质的量减小,CO2的物质的量增大,该比值减小,故A错误;
B、根据图像,达到平衡时消耗c(CO2)=(1.00-0.25)mol·L-1=0.75mol·L-1,则CO2的转化率为0.75/1.00×100%=75%,故B正确;
C、3min时没有达到平衡,即CO2的表示的正反应速率不等于CH3OH表示的逆反应速率,故C错误;
D、根据化学反应速率数学表达式,v(CH3OH)=0.75/10mol/(L·min)=0.075mol/(L·min),根据化学反应速率之比等于化学计量数之比,即v(H2)=3v(CH3OH)=3×0.075mol/(L·min)=0.225mol/(L·min),故D错误。

【题目】草酸(H2C2O4)是一种二元弱酸,广泛分布于动植物体中。
(1)人体内草酸累积过多是导致结石(主要成分是草酸钙)形成的原因之一。有研究发现,EDTA(一种能结合金属离子的试剂)在一定条件下可以有效溶解结石,用化学平衡原理解释其原因:_______________。
(2)已知:0.1 mol·L-1KHC2O4溶液呈酸性。下列说法正确的是_______(填字母序号)。
a. 0.1 mol·L-1KHC2O4溶液中:c(K+) + c(H+) = c(HC2O4-) + 2c(C2O42-) + c(OH-)
b. 0.1 mol·L-1KHC2O4溶液中:c(K+) > c(HC2O4-) > c(C2O42-) > c(H2C2O4)
c. 浓度均为0.1 mol·L-1KHC2O4和K2C2O4的混合溶液中:2c(K+) = c(HC2O4-) + c(C2O42-)
d. 0.1 mol/L KHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+) > c(Na+)
(3)利用草酸制备草酸亚铁晶体(FeC2O4·xH2O)的流程及组分测定方法如下:
![]()
已知:i. pH>4时,Fe2+易被氧气氧化
ii. 几种物质的溶解度(g /100g H2O)如下
FeSO4·7H2O | (NH4)2SO4 | FeSO4·(NH4)2SO4·6H2O | |
20℃ | 48 | 75 | 37 |
60℃ | 101 | 88 | 38 |
①用稀硫酸调溶液pH至1~2的目的是:_____________,______________。
②趁热过滤的原因是:_______________。
③氧化还原滴定法常用于测定草酸亚铁晶体的摩尔质量(M)。称取a g草酸亚铁晶体溶于稀硫酸中,用b mol·L-1的高锰酸钾标准液滴定,到达滴定终点时,消耗高锰酸钾VmL,则M =__________。(已知:部分反应产物为Mn2+、Fe3+、CO2)