题目内容
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是:
A.反应达到平衡时,X的转化率为50%
B.反应达到平衡时,Y的转化率为25%
C.其他条件不变时,增加Y的物质的量,平衡向正反应方向发生移动,平衡常数K变大。
D.其他条件不变时,若温度升高,平衡常数K增大,说明该反应正反应△H<0
| 物质 | X | Y | Z |
| 初始浓度(mol/L) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol/L) | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A.反应达到平衡时,X的转化率为50%
B.反应达到平衡时,Y的转化率为25%
C.其他条件不变时,增加Y的物质的量,平衡向正反应方向发生移动,平衡常数K变大。
D.其他条件不变时,若温度升高,平衡常数K增大,说明该反应正反应△H<0
B、C
试题分析:A、反应达到平衡时,X的转化率为:(0.1mol/L?0.05mol/L)/( 0.1mol/L)×100%=50%,故A正确;
B、反应达到平衡时,Y的转化率为:(0.2mol/L?0.05mol/ L)/( 0.2mol/L)×100%=75%,故B错误;C、平衡常数只跟温度有关,故温度不变,平衡常数不变故,故C错误;D、其他条件不变时,若温度升高,平衡常数K增大,说明该反应正反应△H<0,故D正确。

练习册系列答案
相关题目
 [Fe(SCN)]2+(aq) △H。其中[Fe(SCN)]2+的浓度与温度T的关系如图所示。下列说法正确的是
[Fe(SCN)]2+(aq) △H。其中[Fe(SCN)]2+的浓度与温度T的关系如图所示。下列说法正确的是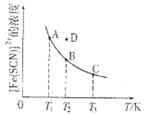
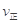 >
>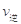
 2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( ) 2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。


 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示: 2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( )
2C(g)一段时间后达到平衡,生成n mol C。则下列说法中不正确的是( )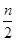 )
)
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1
 O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+
O2(g)=CO2(g) △H2=-283 kJ·mol-1 H2(g)+