题目内容
恒温、恒容的条件下对于N2(g)+3H2(g) 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )| A.断开一个N≡N键的同时有6个N—H键生成 |
| B.混合气体的密度不变 |
| C.混合气体的压强不变 |
| D.N2、H2、NH3分子数之比为1:3 :2的状态 |
C
试题分析:可逆反应达到化学平衡状态的实质是正逆反应速率相等但不为0。会生成断开1个N≡N键的同时,必然会生成2分子氨气,即6个N—H键生成,A不正确。密度是气体的质量和容器体积的比值,反应前后气体质量和容器体积均不变,所以在任何时刻混合气体的密度不变,B不正确。物质的量之比等于压强之比,混合气体的压强不变,说明物质的量也不变化了,既说明达到化学平衡状态了,所以C可以说明。N2、H2、NH3分子数之比1∶3∶2的状态不一定满足正逆反应速率相等,D不正确。答案选C。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
 C(g)+D(g),下列能作为化学平衡状态标志的是:①混合气体的密度;②容器内气体的压强;③混合气体总物质的量;④B的物质的量浓度
C(g)+D(g),下列能作为化学平衡状态标志的是:①混合气体的密度;②容器内气体的压强;③混合气体总物质的量;④B的物质的量浓度 R(g)+S(g)在恒温下已达到平衡是
R(g)+S(g)在恒温下已达到平衡是 CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示: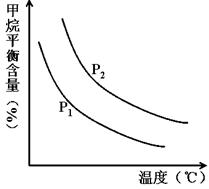
 N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( ) 2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是