题目内容
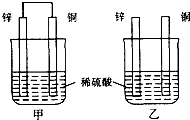
【题目】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,成为化学史上的重要里程碑之一。下列说法中,不正确的是
A. 元素周期表有七个周期
B. 元素周期表有7个主族,7个副族
C. 氧元素位于第二周期ⅥA族
D. 稀有气体元素原子的最外层电子数均为8个
【答案】D
【解析】A.元素周期表有7个横行,则有七个周期,故A正确;B.元素周期表有18个纵行,7个主族、7个副族、1个0族、1个ⅤⅢ族,共16个族,故B正确;C.氧元素的核电荷数为8,位于第二周期ⅥA族,故C正确;D.稀有气体元素包括He,其原子的最外层电子数为2个,故D错误;故选D。

【题目】CH3COOOH(过氧乙酸)广泛应用于环境和医院手术室的消毒,某校化学兴趣小组想利用CH3COOH+H2O2=CH3COOOH+H2O来制取过氧乙酸,查得相关数据如下:
物质 | 沸点 ℃ | 熔点 ℃ | 溶解性 |
CH3COOH | 117.9 | 16.6 | 能溶于水及酒精等有机溶剂 |
H2O2 | 150.2 | -0.43 | 溶于水及酒精 |
CH3COOOH | 105 | 0.1 | 溶于水及酒精等有机溶剂 |
同时查得过氧乙酸具有:刺激性气味,易燃;加热至100℃即猛烈分解;遇火或受热、受震都可引起爆炸;对金属具有较强的腐蚀性。回答以下问题:
(1)利用如图装置进行制取,实验中水浴温度应控制在________100℃(填“>”或“<”或“=”),原因是:____________________________________________________________
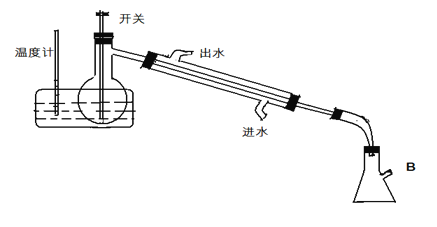
(2)为了使实验顺利进行,B处应接一个_________(填一种装置),然后缓慢打开图中开关通入空气,从而得到过氧乙酸溶液。
(3)实验结束后得到一定量的过氧乙酸,利用如下反应测定该产物的纯度:
2KMnO4+5H2O2 +3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑
2KI+ CH3COOOH+2 H2SO4=2KHSO4+I2+ CH3COOH+H2O
I2+2Na2S2O3=2NaI+Na2S4O6
①取10.00mL制得的过氧乙酸溶液,加水稀释到1000mL,用移液管取20.00mL至锥形瓶中,加入足量稀硫酸酸化后,再用____________(填“酸式滴定管”或“碱式滴定管”)装0.100mol/L的KMnO4溶液进行滴定至_______________________________________现象时恰好完全反应,从而将混在过氧乙酸中的H2O2除去。然后再加入过量KI溶液,加入几滴淀粉,再用0.100mol/L的Na2S2O3滴定消耗了12.00mL。一般工业制得的过氧乙酸质量分数为18% ~ 23%。如果测得实验室制得的过氧乙酸溶液密度为1.15gcm-3。试通过计算判断该溶液是否合格_____________。
②滴定过程中,下列操作会使结果偏大的是_________。
A.滴加Na2S2O3时开始平视滴定管,结束时俯视滴定管。
B.装标准Na2S2O3溶液的滴定管未用标准Na2S2O3溶液润洗。
C.移液管在使用之前未用烘干,里面附着水珠就用来量取待测液
D. .滴加Na2S2O3时开始仰视滴定管,结束时平视滴定管。