籾朕坪否
‐籾朕/斤噐泌和郡哘⇧凪郡哘狛殻議嬬楚延晒幣吭夕泌夕⦿
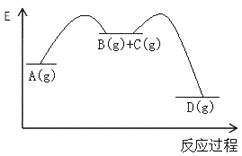
園催 | 郡哘 | 峠財械方 | 郡哘犯 |
郡哘〙 | A(g)=B(g)+C(g) | K1 | @H1 |
郡哘〖 | B(g)+C(g)=D(g) | K2 | @H2 |
郡哘〗 | A(g)= D(g) | K3 | @H3 |
和双傍隈屎鳩議頁
A.K3 ﹆K1 + K2B.@H3﹆@H1+@H2
C.紗岸晒質⇧郡哘〙議郡哘犯週詰⇧郡哘堀楕紗酔D.夸奐寄儿膿⇧K1受弌⇧K2奐寄⇧K3音延
‐基宛/B
‐盾裂/
A、喇郡哘辛岑![]() 、⇧絞K3 ﹆K1 〜 K2⇧危列◉
、⇧絞K3 ﹆K1 〜 K2⇧危列◉
B、喇固帽協舵辛岑@H3﹆@H1 +@H2⇧屎鳩◉
C、岸晒質峪嬬週詰郡哘試晒嬬⇧頁試晒蛍徨為蛍楕奐謹⇧郡哘堀楕紗酔⇧徽音氏唹峒郡哘犯⇧危列◉
D、晒僥峠財械方峪嚥梁業嗤購⇧奐寄儿膿郡哘梁業音延⇧絞光郡哘議峠財械方音延⇧危列◉
基宛僉B。

膳楼過狼双基宛
屢購籾朕