题目内容
【题目】大家都知道,H2S、SO2、NO和CO都是常见的大气污染物,治理污染优化环境对人类的生产与生活尤为重要。
(1)H2S和SO2都是来自硫酸工业的污染物,下列说法正确的是___________。
A .两气体均可以用浓硫酸来干燥 B. 两气体可以用溴水来鉴别
C. 两气体均可以用氢氧化钠溶液来吸收 D. SO2使KMnO4溶液褪色表现出漂白性
(2)汽车尾气的主要成分是氮的氧化物和CO,目前用在汽车的排气管上安装催化转化装置,发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) 来除去这两种污染物。有人设想按下列反应:2CO(g)=2C(s)+O2(g)来除去CO,已知该反应为吸热反应,则该设想能否实现___选填“能”或“不能”),理由是_______________________________________。
N2(g)+2CO2(g) 来除去这两种污染物。有人设想按下列反应:2CO(g)=2C(s)+O2(g)来除去CO,已知该反应为吸热反应,则该设想能否实现___选填“能”或“不能”),理由是_______________________________________。
(3)为减少SO2的排放,常采用的措施是,将煤转化为清洁气体燃料。
已知:
2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
2C(s) + O2(g)=2CO(g) △H=-221kJ/mol
请写出焦炭与水蒸气反应的热化学方程式________________。
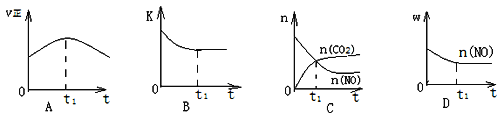
(4)根据(2)中汽车尾气净化原理,若该反应为放热反应,且该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应进行到t1时刻时达到平衡状态的是____。(填序号,下图中的v正、K、n、W分别表示正反应速率、平衡常数、物质的量、质量分数。)
【答案】 BC 不能 反应能发生的条件是:△G=△H-T△S<0,而该反应的△H>0,△S<0,所以△G>0 C(S) + H2O(g)=CO(g)+H2(g) △H=+131.3kJ/mol BD
【解析】(1)A .H2S能被浓硫酸氧化,不能用浓硫酸来干燥,A错误;B. H2S与溴水反应生成单质硫沉淀,SO2与溴水反应生成硫酸和溴化氢,因此两气体可以用溴水来鉴别,B正确;C. 两气体均可以用氢氧化钠溶液来吸收,C正确;D. SO2使KMnO4溶液褪色表现出还原性,D错误,答案选BC;(2)由于反应能发生的条件是:△G=△H-T△S<0,而该反应的△H>0,△S<0,所以△G>0,因此该设想不能实现。(3)已知:
①2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
②2C(s) + O2(g)=2CO(g) △H=-221kJ/mol
根据盖斯定律可知(②-①)/2即得到焦炭与水蒸气反应的热化学方程式为C(s) + H2O(g)=CO(g)+H2(g) △H=+131.3kJ/mol。(4)A、t1时正反应速率仍然在变化,说明没有达到平衡状态,A错误;B、t1时平衡常数不再变化,正逆反应速率相等,说明达到了平衡状态,B正确;C、t1时二氧化碳和一氧化氮的物质的量还在变化,说明正逆反应速率不相等,反应没有达到平衡状态,C错误;D、t1时一氧化氮的质量分数不再变化,表明正逆反应速率相等,达到了平衡状态,D正确;答案选BD。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案