题目内容
【题目】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( ) 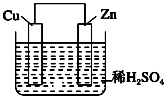
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为0.5mol;
⑥正极的电极反应式为Zn﹣2e﹣═Zn2+ .
A.①②③
B.③④⑤
C.④⑤⑥
D.②③④
【答案】B
【解析】解:①Zn为负极,Cu为正极,故①错误;
②H+向正极移动,故②错误;
③电子由Zn电极流向Cu电极,故③正确;
④Cu电极上发生2H++2e﹣=H2↑,故④正确;
⑤由2H++2e﹣=H2↑可知,有1mol电子流向导线,产生氢气0.5mol,故⑤正确;
⑥正极反应为2H++2e﹣=H2↑,故⑥错误;
故选B.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
【题目】在一定条件下,N2O分解的部分实验数据如下( )
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/molL-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
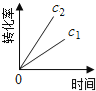
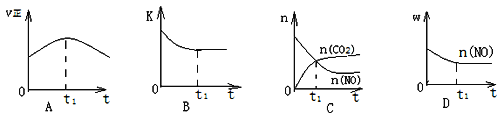
下图能正确表示该反应有关物理量变化规律的是( )
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
A. B.
B. C.
C. D.
D.