题目内容
下列溶液中有关微粒的物质的量浓度或物理量关系正确的是( )
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HR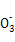 )+2c(R )+2c(R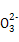 ) ) |
| B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) |
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(N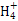 ):①<③<② ):①<③<② |
| D.等体积等物质的量浓度的NaClO溶液与NaCl溶液中离子总数:N前>N后 |
A
选项A中混合液中的电荷守恒式为c(H+)+c(Na+)=c(OH-)+c(HR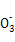 )+2c(R
)+2c(R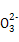 ),在中性溶液中c(H+)=c(OH-),因此选项A正确。选项B同样可以先写出混合溶液中的电荷守恒式:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),又由于溶液呈中性,即c(H+)=c(OH-),因此混合溶液中应有c(Na+)=c(Cl-)+c(CH3COO-),根据物料守恒可得c(Na+)=c(CH3COOH)+c(CH3COO-),所以有c(Na+)>c(Cl-)=c(CH3COOH),选项B错误。对于选项C,Fe2+的存在会抑制N
),在中性溶液中c(H+)=c(OH-),因此选项A正确。选项B同样可以先写出混合溶液中的电荷守恒式:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),又由于溶液呈中性,即c(H+)=c(OH-),因此混合溶液中应有c(Na+)=c(Cl-)+c(CH3COO-),根据物料守恒可得c(Na+)=c(CH3COOH)+c(CH3COO-),所以有c(Na+)>c(Cl-)=c(CH3COOH),选项B错误。对于选项C,Fe2+的存在会抑制N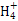 的水解,C
的水解,C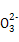 的存在会促进N
的存在会促进N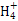 的水解,因此选项C错误。根据电荷守恒可知选项D是错误的。
的水解,因此选项C错误。根据电荷守恒可知选项D是错误的。
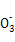 )+2c(R
)+2c(R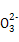 ),在中性溶液中c(H+)=c(OH-),因此选项A正确。选项B同样可以先写出混合溶液中的电荷守恒式:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),又由于溶液呈中性,即c(H+)=c(OH-),因此混合溶液中应有c(Na+)=c(Cl-)+c(CH3COO-),根据物料守恒可得c(Na+)=c(CH3COOH)+c(CH3COO-),所以有c(Na+)>c(Cl-)=c(CH3COOH),选项B错误。对于选项C,Fe2+的存在会抑制N
),在中性溶液中c(H+)=c(OH-),因此选项A正确。选项B同样可以先写出混合溶液中的电荷守恒式:c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(CH3COO-),又由于溶液呈中性,即c(H+)=c(OH-),因此混合溶液中应有c(Na+)=c(Cl-)+c(CH3COO-),根据物料守恒可得c(Na+)=c(CH3COOH)+c(CH3COO-),所以有c(Na+)>c(Cl-)=c(CH3COOH),选项B错误。对于选项C,Fe2+的存在会抑制N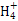 的水解,C
的水解,C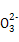 的存在会促进N
的存在会促进N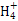 的水解,因此选项C错误。根据电荷守恒可知选项D是错误的。
的水解,因此选项C错误。根据电荷守恒可知选项D是错误的。
练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目