题目内容
工业上常用NaClO3和Na2SO3溶液混合,并加H2SO4酸化后反应制取一种广谱消毒剂,在该反应中NaClO3和Na2SO3的物质的量之比为2:1,该广谱消毒剂的化学式为
- A.Cl2O7
- B.ClO2
- C.Cl2O3
- D.Cl2O
B
分析:根据题意“工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得”,由此可知,NaClO3中氯元素的化合价由+5价降低,反应中NaClO3为氧化剂,则Na2SO3为还原剂,被氧化为Na2SO4,根据电子转移守恒计算Cl元素在还原产物中的化合价,据此判断.
解答:根据题意“工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得”,由此可知,NaClO3中氯元素的化合价由+5价降低,反应中NaClO3为氧化剂,则Na2SO3为还原剂,则Na2SO3被氧化生成+6价S,生成Na2SO4,令Cl元素在还原产物中的化合价为a,则:2×(5-a)=1×(6-4),解得a=4,故该广谱消毒剂的化学式为ClO2,故选B.
点评:本题考查氧化还原反应的有关计算,难度不大,注意从化合价变化判断氧化剂、还原剂、氧化产物、还原产物等概念,利用电子转移守恒计算.
分析:根据题意“工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得”,由此可知,NaClO3中氯元素的化合价由+5价降低,反应中NaClO3为氧化剂,则Na2SO3为还原剂,被氧化为Na2SO4,根据电子转移守恒计算Cl元素在还原产物中的化合价,据此判断.
解答:根据题意“工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得”,由此可知,NaClO3中氯元素的化合价由+5价降低,反应中NaClO3为氧化剂,则Na2SO3为还原剂,则Na2SO3被氧化生成+6价S,生成Na2SO4,令Cl元素在还原产物中的化合价为a,则:2×(5-a)=1×(6-4),解得a=4,故该广谱消毒剂的化学式为ClO2,故选B.
点评:本题考查氧化还原反应的有关计算,难度不大,注意从化合价变化判断氧化剂、还原剂、氧化产物、还原产物等概念,利用电子转移守恒计算.

练习册系列答案
相关题目
 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是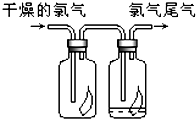 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现是