题目内容
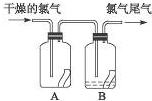 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是潮湿的有色布条褪色而干燥的有色布条不褪色
潮湿的有色布条褪色而干燥的有色布条不褪色
.(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用
NaOH
NaOH
溶液吸收多余的氯气,原理是(用化学方程式表示)2NaOH+Cl2═NaClO+NaCl+H2O
2NaOH+Cl2═NaClO+NaCl+H2O
.根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是Ca(ClO)2
Ca(ClO)2
(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是C
C
(用字母代号填).A.O2 B.Cl2 C.CO2 D.HClO.
分析:(1)次氯酸能使有色布条褪色;
(2)氯水显酸性,可以用碱性物质吸收;氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,次氯酸钙和二氧化碳反应生成碳酸钙,碳酸钙和盐酸反应生成二氧化碳.
(2)氯水显酸性,可以用碱性物质吸收;氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,次氯酸钙和二氧化碳反应生成碳酸钙,碳酸钙和盐酸反应生成二氧化碳.
解答:解:(1)氯气没有漂白性,所以干燥的氯气不能使有色布条褪色,氯气和水反应生成盐酸和次氯酸,次氯酸有强氧化性而使有色布条褪色,所以看到的现象是A中有色布条不褪色,B中有色布条褪色,
故答案为:潮湿的有色布条褪色而干燥的有色布条不褪色;
(2)氯水显酸性,可以用碱性物质氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应方程式为:2NaOH+Cl2═NaClO+NaCl+H2O;氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,漂白粉的有效成分是Ca(ClO)2,次氯酸钙和二氧化碳反应生成碳酸钙,碳酸钙和盐酸反应生成二氧化碳,所以长期露置于空气中的漂白粉,加稀盐酸后产生的气体是二氧化碳,故选C,
故答案为:NaOH;2NaOH+Cl2═NaClO+NaCl+H2O;Ca(ClO)2; C.
故答案为:潮湿的有色布条褪色而干燥的有色布条不褪色;
(2)氯水显酸性,可以用碱性物质氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应方程式为:2NaOH+Cl2═NaClO+NaCl+H2O;氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,漂白粉的有效成分是Ca(ClO)2,次氯酸钙和二氧化碳反应生成碳酸钙,碳酸钙和盐酸反应生成二氧化碳,所以长期露置于空气中的漂白粉,加稀盐酸后产生的气体是二氧化碳,故选C,
故答案为:NaOH;2NaOH+Cl2═NaClO+NaCl+H2O;Ca(ClO)2; C.
点评:本题考查了次氯酸的漂白性、氯气的性质,知道次氯酸漂白性原理,会根据氯气和水反应原理分析氯气和碱溶液反应原理,注意次氯酸是强氧化性弱酸.

练习册系列答案
相关题目
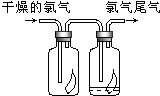 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现是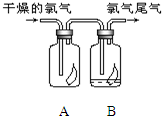 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是