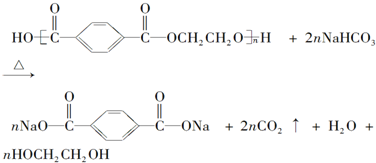
题目内容
15.实验操作的规范是实验的基本要求.下列实验操作正确的是( )| A. | 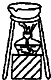 蒸发食盐水 | B. |  用量筒量取液体 | C. |  测溶液的pH | D. | 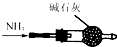 干燥NH3 |
分析 A.外焰温度最高;
B.100mL量筒精确到1mL;
C.不能将pH试纸伸入待测液中,以免污染待测液;
D.氨气可用碱石灰干燥.
解答 解:A.外焰温度最高,应用外焰加热,故A错误;
B.100mL量筒精确到1mL,无法量取9.5mL液体,故B错误;
C.用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,故C错误;
D.氨气呈碱性,氨气可用碱石灰干燥,故D正确.
故选D.
点评 本题考查化学实验方案的评价,难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
5.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 2.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.04NA | |
| C. | 7.8g Na2S和Na2O2的固体混合物中含有的阴离子数等于0.1NA | |
| D. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
6.下列叙述中,正确的是( )
| A. | 1s电子云界面图是一个球面,电子云中的每个小黑点代表一个电子 | |
| B. | NaH中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠形成的 | |
| C. | 对于组成结构相似的分子,一定是相对分子质量越大,熔、沸点越高 | |
| D. | 在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析 |
3.实验操作的规范是实验的基本要求.下列实验操作正确的是( )
| A. | 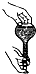 检查容量瓶是否漏水 | B. |  给溶液加热 | ||
| C. | 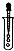 滴加液体 | D. | 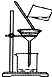 过滤 |
10.下列变化中,涉及不到化学变化的是( )
| A. | 石油的分馏 | B. | 氯气溶于水 | C. | 食物腐败 | D. | 煤的干馏 |
20.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 56gN2和CO的混合气体中含有的原子总数目为2NA | |
| B. | 标准状况下,11.2L乙醇中含有的分子数目为0.5NA | |
| C. | 1L1mol•L-1 MgCl2溶液中含有的氯离子数目为NA | |
| D. | 2.7gAl粉在足量的Cl2中完全燃烧转移的电子数目为0.3NA |
7.某同学进行实验研究时,欲配制1.0mol•L-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2•8H2O试剂(化学式量:315).在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物.为探究其原因,该同学查得Ba(OH)2•8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6.
(1)烧杯中未溶物可能仅为BaCO3,理由是Ba(OH)2•8H2O与CO2作用转化为BaCO3.
(2)假设试剂由大量Ba(OH)2•8H2O和少量BaCO3组成.设计实验方案,进行成分检
验.写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管带塞导气管、滴管
(3)将试剂初步提纯后,准确测定其中Ba(OH)2•8H2O的含量.实验如下:
①配制250mL约0.1mol•L-1 Ba(OH)2溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,溶解,将溶液转入250ml的容量瓶中,洗涤,定容,摇匀.
②滴定:准确量取25.00mL所配Ba(OH)2溶液于锥形瓶中,滴加指示剂,将0.1980(填“0.0210”、“0.0536”、“0.1980”或“1.5000”)mol•L-1盐酸装入50mL酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸V mL.
③计算Ba(OH)2•8H2O的质量分数=$\frac{0.25L×\frac{0.198V}{50}mol×315g/mol}{wg}$×100%(只列出算式,不做运算).
(4)室温下,不能(填“能”或“不能”) 配制1.0 mol•L-1 Ba(OH)2溶液.
(1)烧杯中未溶物可能仅为BaCO3,理由是Ba(OH)2•8H2O与CO2作用转化为BaCO3.
(2)假设试剂由大量Ba(OH)2•8H2O和少量BaCO3组成.设计实验方案,进行成分检
验.写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
| 步骤2:取适量滤液于试管中,滴加稀硫酸. | |
| 步骤3:取适量步骤1中的沉淀于试管中,取适量步骤1中的沉淀于试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中. | |
| 步骤4:取适量滤液于烧杯中,用pH计测其 pH值 |
①配制250mL约0.1mol•L-1 Ba(OH)2溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,溶解,将溶液转入250ml的容量瓶中,洗涤,定容,摇匀.
②滴定:准确量取25.00mL所配Ba(OH)2溶液于锥形瓶中,滴加指示剂,将0.1980(填“0.0210”、“0.0536”、“0.1980”或“1.5000”)mol•L-1盐酸装入50mL酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸V mL.
③计算Ba(OH)2•8H2O的质量分数=$\frac{0.25L×\frac{0.198V}{50}mol×315g/mol}{wg}$×100%(只列出算式,不做运算).
(4)室温下,不能(填“能”或“不能”) 配制1.0 mol•L-1 Ba(OH)2溶液.
4.下列仪器中,不能加热使用的是( )
| A. | 锥形瓶 | B. | 试管 | C. | 容量瓶 | D. | 烧杯 |