题目内容
HCN无色有杏仁气味的有毒气体,早期广泛用于船舱、仓库的烟熏灭鼠。
已知:HCN( aq)与NaOH(aq)反应的焓变ΔH=-12.1 kJ·mol-1; HCl(aq)与NaOH(aq)反应的焓变ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的焓变ΔH等于
已知:HCN( aq)与NaOH(aq)反应的焓变ΔH=-12.1 kJ·mol-1; HCl(aq)与NaOH(aq)反应的焓变ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的焓变ΔH等于
| A.-67.7 kJ·mol-1 | B.-43.5 kJ·mol-1 |
| C.+43.5 kJ·mol-1 | D.+67.7 kJ·mol-1 |
C
试题分析:根据能量守恒定律可知,HCN在水溶液中电离的焓变ΔH等于-12.1 kJ·mol-1+55.6 kJ·mol-1=+43.5 kJ·mol-1,答案选C。
点评:该题是基础性试题的考查,难度不大,试题注重基础,兼顾能力的培养。有利于培养学生的逻辑推理能力和灵活应变能力。该题的关键是借助于能量守恒定律。

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目


 2NO(g)
2NO(g)  H>0
H>0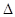 H=-67.7 kJ·mol-1
H=-67.7 kJ·mol-1 F-(aq)+H+(aq)
F-(aq)+H+(aq)  2NH3(g)△H=-92.0KJ·mol-1,将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,反应达到平衡时的热量变化是
2NH3(g)△H=-92.0KJ·mol-1,将1mol N2和3mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时在该容器中充入2mol NH3,反应达到平衡时的热量变化是