题目内容
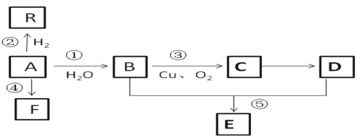
【题目】A 是一种来自石油的重要的有机物,也是果实催熟剂。D 和 C 碳原子数相同,其水溶液能使紫色石蕊变红。E 是一种具有果香味的酯,F 是一种高聚物,可制成多种包装材料。相互转化如下:
(1)B 的分子式为______,D 的官能团为________。
(2) 写出反应①、⑤的化学方程式:①__,反应类型为 ______;⑤_,反应类型为_______。
(3)R 的一种同系物 W,相对分子质量比R 大 154,则W的分子式为_________。
(4)与A 相邻的同系物 Q 与溴水反应的化学方程式为_______。
【答案】C2H6O 羧基 CH2=CH2+H2O![]() CH3CH2OH 加成反应 CH3CH2OH+CH3COOH
CH3CH2OH 加成反应 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 取代反应 C13H28 CH3CH=CH2+Br2→CH3CHBrCH2Br
CH3COOCH2CH3+H2O 取代反应 C13H28 CH3CH=CH2+Br2→CH3CHBrCH2Br
【解析】
A是一种来自石油的重要的有机物,也是果实催熟剂,则A为CH2=CH2,A与H2发生加成反应生成R,则R为CH3CH3,A与H2O发生加成反应生成B,则B为CH3CH2OH,B发生催化氧化生成C,C为CH3CHO,D和C碳原子数相同,其水溶液能使紫色石蕊变红,则D为CH3COOH,B与D反应生成E,E是一种具有果香味的酯,则E为CH3COOCH2CH3,F是一种高聚物,则F为聚乙烯,据此分析解答。
(1)根据上述分析可知,B为CH3CH2OH,B的分子式为C2H6O,D为CH3COOH,其官能团为羧基,故答案为:C2H6O;羧基;
(2)反应①为CH2=CH2与H2O发生加成反应生成CH3CH2OH,反应的化学方程式为CH2=CH2+H2O![]() CH3CH2OH,反应⑤为CH3CH2OH和CH3COOH发生酯化(取代)反应生成CH3COOCH2CH3,反应的化学方程式为CH3CH2OH+CH3COOH
CH3CH2OH,反应⑤为CH3CH2OH和CH3COOH发生酯化(取代)反应生成CH3COOCH2CH3,反应的化学方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O,故答案为:CH2=CH2+H2O
CH3COOCH2CH3+H2O,故答案为:CH2=CH2+H2O![]() CH3CH2OH;加成反应;CH3CH2OH+CH3COOH
CH3CH2OH;加成反应;CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;取代反应;
CH3COOCH2CH3+H2O;取代反应;
(3)R的分子式为C2H6,其同系物W的相对分子质量比R大154,则W比R多![]() 个“CH2”,因此W的分子式为C13H28,故答案为:C13H28;
个“CH2”,因此W的分子式为C13H28,故答案为:C13H28;
(4)与A相邻的同系物Q为CH3CH=CH2,其与溴水反应生成1,2-二溴丙烷,反应的化学方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br,故答案为:CH3CH=CH2+Br2→CH3CHBrCH2Br。

 名校课堂系列答案
名校课堂系列答案