题目内容
【题目】有关物质的转化关系如下图所示。A、C、E是常见的金属单质,E为紫红色,反应①可用于焊接铁轨,B是赤铁矿的主要成分,F的溶液中加入KSCN溶液变红。(部分反应物和生成物省略)
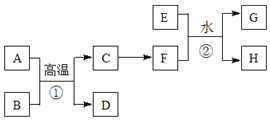
请回答下列问题:
(1)B的化学式是____________D的化学式是_____________
(2)可选用__________(填“字母”)实现反应C→F的转化。
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为___________________________。
(4)反应②的离子方程式为___________________________。
【答案】Fe2O3 Al2O3 b 2Al+ Fe2O3![]() 2Fe + Al2O3 2Fe3+ +Cu=Cu2++2Fe2+
2Fe + Al2O3 2Fe3+ +Cu=Cu2++2Fe2+
【解析】
A、C、E是常见的金属单质,反应①可用于焊接铁轨,B是赤铁矿的主要成分,则A为Al、B为Fe2O3,C为Fe,D为Al2O3,E是紫红色的金属单质,则E为Cu,F的溶液中加入KSCN溶液变红,F为铁盐,可以由Fe与氯气反应得到,反应②为Cu+2Fe3+=Cu2++2Fe2+,据此分析解答。
根据上述分析,A为Al、B为Fe2O3,C为Fe,D为Al2O3,E为Cu,F为铁盐。
(1)B的化学式为Fe2O3,D的化学式为Al2O3,故答案为:Fe2O3;Al2O3;
(2)反应C→F是Fe转化为Fe3+,Fe与盐酸、CuSO4溶液生成Fe2+,Fe与氯气反应生成 FeCl3,故答案为:b;
(3)反应①为铝热反应,反应的化学方程式为:2Al+Fe2O3 ![]() 2Fe+Al2O3,故答案为:2Al+Fe2O3
2Fe+Al2O3,故答案为:2Al+Fe2O3 ![]() 2Fe+Al2O3;
2Fe+Al2O3;
(4)反应②为铁盐与铜的反应,反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,故答案为:Cu+2Fe3+=Cu2++2Fe2+。

【题目】工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
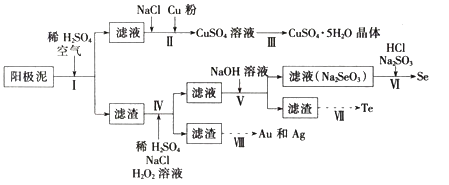
已知:①阳极泥的主要化学成分,如表所示:
主要成分 | Cu Ag Au Se Te |
百分含量/% | 23.4 12.1 0.9 6.7 3.1 |
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示:
固定浸出温度 | 固定H2SO4浓度 | |||
H2SO4浓度 / mol·L-1 | 浸出率/% | 浸出温度/℃ | 浸出率/% | |
Cu Ag Au Se Te | Cu Ag Au Se Te | |||
4 | 95.1 4.67 <0.2 0.83 8.93 | 30 | 87.1 4.58 <0.2 0.08 6.83 | |
3 | 94.5 4.65 <0.2 0.28 6.90 | 40 | 94.5 4.65 <0.2 0.28 6.90 | |
2 | 78.1 2.65 <0.2 0.05 2.85 | 50 | 96.1 5.90 <0.2 0.64 8.73 |
(1)步骤I的主要目的为浸出铜,发生的主要反应的化学方程式为__________;分析表2数据,可知步骤I最适合的条件为______________。
(2)步骤II中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为________。
(3)步骤III的操作方法为___________。
(4)步骤IV中,反应温度为75℃。加入H2O2溶液作用为______________;此过程中H2O2溶液的添加量要远远高于理论值,原因为_____________。
(5)步骤VI中所发生反应的化学方程式为_______。
(6)步骤VII中,碱性环境下电解Na2TeO3溶液可得Te实现,阴极的电极反应式为_____。