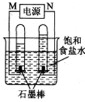
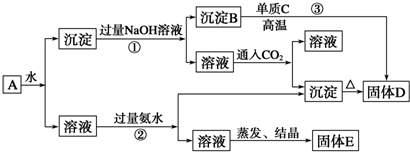
题目内容
 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=260kJ?mol-1
已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1则CH4与O2反应生成CO和H2的热化学方程式为:
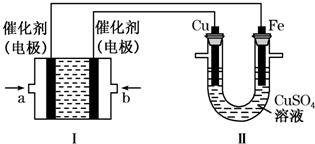
(2)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜.
①a处应通入
②电镀结束后,装置Ⅰ中溶液的pH
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷
考点:原电池和电解池的工作原理
专题:
分析:(1)根据盖斯定律书写热化学反应方程式;
(2)①II中首先镀铜,则Cu作阳极、Fe作阴极,I中a处电极为负极、b处电极为正极,负极上通入燃料、正极上通入氧化剂;甲烷失电子和氢氧根离子反应生成碳酸根离子和水;
②根据I中氢氧根离子浓度变化确定溶液pH变化;II中发生电镀,阳极上溶解的铜质量等于阴极上析出铜的质量;
③I中还有碳酸根离子生成;
④根据转移电子相等计算消失甲烷的体积.
(2)①II中首先镀铜,则Cu作阳极、Fe作阴极,I中a处电极为负极、b处电极为正极,负极上通入燃料、正极上通入氧化剂;甲烷失电子和氢氧根离子反应生成碳酸根离子和水;
②根据I中氢氧根离子浓度变化确定溶液pH变化;II中发生电镀,阳极上溶解的铜质量等于阴极上析出铜的质量;
③I中还有碳酸根离子生成;
④根据转移电子相等计算消失甲烷的体积.
解答:
解:(1)CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=260kJ?mol-1①
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1②,
将方程式2①+②得 2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=-46kJ?mol-1 ,
故答案为:2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=-46kJ?mol-1 ;
(2)①II中首先镀铜,则Cu作阳极、Fe作阴极,I中a处电极为负极、b处电极为正极,负极上通入燃料、正极上通入氧化剂,所以a处通入的气体是甲烷;甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应为CH4+10OH--8e-=CO32-+7H2O,
故答案为:甲烷;CH4+10OH--8e-=CO32-+7H2O;
②根据I中电池反应为CH4+2O2+2KOH=K2CO3+3H2O,KOH参加反应导致溶液中KOH浓度降低,则溶液的pH减小;
II中发生电镀,阳极上溶解的铜质量等于阴极上析出铜的质量,则溶液中铜离子浓度不变,
故答案为:变小;不变;
③I中负极反应为CH4+10OH--8e-=CO32-+7H2O,所以还有碳酸根离子生成,故答案为:CO32-;
④串联电路中转移电子相等,所以消耗甲烷的体积=
×22.4L/mol=1.12L,故答案为:1.12.
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1②,
将方程式2①+②得 2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=-46kJ?mol-1 ,
故答案为:2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=-46kJ?mol-1 ;
(2)①II中首先镀铜,则Cu作阳极、Fe作阴极,I中a处电极为负极、b处电极为正极,负极上通入燃料、正极上通入氧化剂,所以a处通入的气体是甲烷;甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应为CH4+10OH--8e-=CO32-+7H2O,
故答案为:甲烷;CH4+10OH--8e-=CO32-+7H2O;
②根据I中电池反应为CH4+2O2+2KOH=K2CO3+3H2O,KOH参加反应导致溶液中KOH浓度降低,则溶液的pH减小;
II中发生电镀,阳极上溶解的铜质量等于阴极上析出铜的质量,则溶液中铜离子浓度不变,
故答案为:变小;不变;
③I中负极反应为CH4+10OH--8e-=CO32-+7H2O,所以还有碳酸根离子生成,故答案为:CO32-;
④串联电路中转移电子相等,所以消耗甲烷的体积=
| ||
| 8 |
点评:本题考查了盖斯定律、原电池和电解池原理,根据电解池中Cu、Fe电极上发生的反应确定燃料电池中正负极及电极上通入的气体,再结合转移电子相等计算,难点是电极反应式的书写.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
下列化学用语正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、葡萄糖的结构式:C6H12O6 |
C、顺-2-丁烯的结构简式: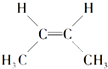 |
| D、乙酸的实验式:C2H4O2 |
下列各溶液中能大量共存的离子组是( )
| A、使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO32-、K+ |
| B、使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C、使石蕊试液呈蓝色的溶液中:Na+、NH4+、S2-、SO32- |
| D、在pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl- |