题目内容
根据乙烯的实验室制法,请回答以下相关问题:
(1)实验室制取乙烯反应原理 (写出相关方程式)
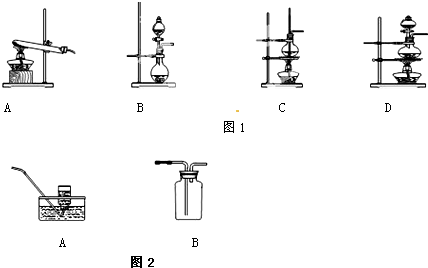
(2)根据反应原理从图1中找出制取乙烯的装置 (填序号)
(3)浓硫酸的作用是
(4)为了防止混合液在受热时暴沸应如何处理
(5)制取乙烯温度宜控制在170℃左右,温度过低,如140℃则发生的副反应是 (写出相关方程式)
(6)收集气体常用方法如图2所示,收集乙烯应该选用 (填序号)

(1)实验室制取乙烯反应原理
(2)根据反应原理从图1中找出制取乙烯的装置
(3)浓硫酸的作用是
(4)为了防止混合液在受热时暴沸应如何处理
(5)制取乙烯温度宜控制在170℃左右,温度过低,如140℃则发生的副反应是
(6)收集气体常用方法如图2所示,收集乙烯应该选用
考点:乙烯的实验室制法
专题:有机物的化学性质及推断
分析:(1)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯;
(2)根据乙醇制取乙烯的反应条件进行分析;
(3)根据乙醇制取乙烯的反应原理进行分析;
(4)反应条件是加热到170℃,因乙醇的沸点低,易暴沸,所以加沸石;
(5)温度在140℃,乙醇在浓硫酸作用下发生分子间脱水,会有乙醚生成;
(6)根据气体的性质选择收集气体的装置;
(2)根据乙醇制取乙烯的反应条件进行分析;
(3)根据乙醇制取乙烯的反应原理进行分析;
(4)反应条件是加热到170℃,因乙醇的沸点低,易暴沸,所以加沸石;
(5)温度在140℃,乙醇在浓硫酸作用下发生分子间脱水,会有乙醚生成;
(6)根据气体的性质选择收集气体的装置;
解答:
解:(1)乙醇与浓硫酸混合加热到170℃发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH
CH2=CH2↑+H2O;
故答案为:CH3CH2OH
CH2=CH2↑+H2O;
(2)实验室中用乙醇和浓硫酸反应制取乙烯的反应为:CH3CH2OH
CH2=CH2↑+H2O为液体和液体加热制取气体,不能使用A装置,该反应的温度为170℃,不能使用B装置,为了控制反应温度,需要使用温度计,装置D中没有温度计,故C错误,故A、B、D错误;所以正确的装置为C,
故答案为:C;
(3)浓硫酸不是反应物,是催化剂,反应中加快CH3CH2OH分子内脱水生成乙烯,所以浓硫酸起到催化剂和脱水剂的作用,
故答案为:催化剂和脱水剂;
(4)因乙醇的沸点低,易暴沸,所以加入沸瓷片作沸石,防暴沸,
故答案为:加沸石;
(5)乙醇在浓硫酸作用下加热到140℃会发生分子间脱水2C2H5OH
C2H5-O-C2H5+H2O生成乙醚,
故答案为:2C2H5OH
C2H5-O-C2H5+H2O;
(6)乙烯密度与空气接近,不溶于水,不和水发生反应,所以选用排水法收集,
故选A.
| 浓硫酸 |
| 170℃ |
故答案为:CH3CH2OH
| 浓硫酸 |
| 170℃ |
(2)实验室中用乙醇和浓硫酸反应制取乙烯的反应为:CH3CH2OH
| 浓硫酸 |
| 170℃ |
故答案为:C;
(3)浓硫酸不是反应物,是催化剂,反应中加快CH3CH2OH分子内脱水生成乙烯,所以浓硫酸起到催化剂和脱水剂的作用,
故答案为:催化剂和脱水剂;
(4)因乙醇的沸点低,易暴沸,所以加入沸瓷片作沸石,防暴沸,
故答案为:加沸石;
(5)乙醇在浓硫酸作用下加热到140℃会发生分子间脱水2C2H5OH
| 浓硫酸 |
| 140℃ |
故答案为:2C2H5OH
| 浓硫酸 |
| 140℃ |
(6)乙烯密度与空气接近,不溶于水,不和水发生反应,所以选用排水法收集,
故选A.
点评:本题考查实验室制取乙烯,题目难度不大,明确反应原理是解题关键,注意乙醇在浓硫酸作用下加热到140℃会发生分子间脱水生成乙醚的反应原理.

练习册系列答案
相关题目
将2mol A和2mol B通入一密闭容器中,在某温度下达到平衡:2A(g)+B(g)?2C(g)+D(g).经测定,平衡时混合气体中C的体积分数为24%,则B的转化率为( )
| A、73% | B、24% |
| C、36% | D、12% |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、11g T216O含有的中子数为6NA |
| B、1mol Na2O2与CO2完全反应转移的电子数为2NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、标准状况下,2.24L H2O所含共价键数为0.2NA |
下列表述不正确的是( )
| A、福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同 |
| B、电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述 |
| C、凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
| D、钠原子L层共有8种运动状态不同的电子 |
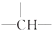 和一个-Cl,它的可能结构分别是
和一个-Cl,它的可能结构分别是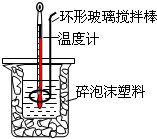 测定中和热实验装置如图:
测定中和热实验装置如图: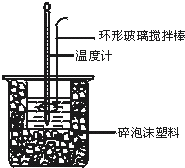 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: