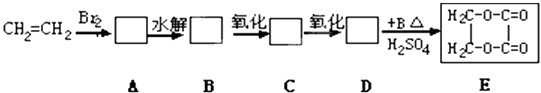
��Ŀ����
����Ŀ�����ĵ��ʼ��仯�������ʶ�������;�㷺�� ���������գ�
��1����ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2��2NO+2CO ![]() 2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
c��CO�� | 3.60��10��3 | 3.05��10��3 | 2.85��10��3 | 2.75��10��3 | 2.70��10��3 | 2.70��10��3 |
�÷�Ӧƽ�ⳣ��K�ı���ʽΪ���¶����ߣ�Kֵ��ѡ���������С���������䡱����ǰ2s�ڵ�ƽ����Ӧ����v��N2��=����������Ӧ���ܱ������з������ﵽƽ��ʱ�����NOת���ʵĴ�ʩ֮һ�� ��
��2����ҵ�ϳɰ��ķ�Ӧ�¶�ѡ��500�����ҵ�ԭ���� ��
��3��ʵ�����ڹ̶��ݻ����ܱ������м���1mol������3mol����ģ�ҵ�ϳɰ�����Ӧ��һ���������Ѵﵽƽ��ı�־�� �� a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2
b�������ڵ�ѹǿ���ֲ���
c��N2��H2��NH3��Ũ�Ȳ��ٷ����仯
d����Ӧֹͣ�������淴Ӧ�����ʶ�������
��4����������1mol���ʵ�ϡ�����л���ͨ��1mol NH3����Һ����仯���Բ��ƣ�����Ӧ��������Һ������Ũ���ɴ�С��˳��������ͨ��NH3�Ĺ�������Һ�ĵ���������ѡ��������С�������������䡱����
���𰸡�
��1��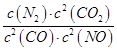 ����С��1.875��10��4mol/��L?s��������ѹǿ
����С��1.875��10��4mol/��L?s��������ѹǿ
��2��������500�����Ҿ�����ѻ���
��3��bc
��4��c��Cl��������NH4+����c��H+����c��OH��������������
���������⣺��1������ƽ�ⳣ������������Ũ�ȵ�ϵ������֮�����Է�ӦŨ��ϵ������֮��������K= ![]() ���÷�ӦΪ���ȷ�Ӧ���¶�ʱƽ�������ƶ�������ƽ�ⳣ����С��v��CO��=
���÷�ӦΪ���ȷ�Ӧ���¶�ʱƽ�������ƶ�������ƽ�ⳣ����С��v��CO��= ![]() =
= ![]() =3.75��10��4mol/l��v��N2��=
=3.75��10��4mol/l��v��N2��= ![]() =1.875��10��4mol/��Ls����һ��������ת���ʱ��˵��ƽ�������ƶ�����ͨ���ı�ѹǿ��ʹƽ�������ƶ����ʴ�Ϊ��
=1.875��10��4mol/��Ls����һ��������ת���ʱ��˵��ƽ�������ƶ�����ͨ���ı�ѹǿ��ʹƽ�������ƶ����ʴ�Ϊ�� ![]() ����С��1.875��10��4mol/��Ls��������ѹǿ����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ���ʴ��Ϊ��������500�����Ҿ�����ѻ��ԣ���3��a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2�������Dz��䣬�ʴ���
����С��1.875��10��4mol/��Ls��������ѹǿ����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ���ʴ��Ϊ��������500�����Ҿ�����ѻ��ԣ���3��a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2�������Dz��䣬�ʴ���
b�������ڵ�ѹǿ���ֲ��䣬˵����������ʵ������䣬��Ӧ��ƽ��״̬������ȷ��
c��N2��H2��NH3��Ũ�Ȳ��ٷ����仯��˵�����淴Ӧ������ȣ���Ӧ��ƽ��״̬������ȷ��
d����ѧƽ��״̬�Ƕ�̬ƽ�⣬��Ӧ������ֹͣ���ʴ���
��ѡ��bc����4������ǡ�÷�Ӧ�����Ȼ�泥���Һ�����ԣ���c��H+����c��OH������������Һ�ʵ������У�c��H+��+c��NH4+��=c��OH����+c��Cl��������Ϊc��H+����c��OH��������c��NH4+����c��Cl������������Ũ�ȴ�С��ϵΪ��c��Cl��������NH4+����c��H+����c��OH��������Һ������Ũ�ȼ������䣬���Ե��������������䣬�ʴ�Ϊ��c��Cl��������NH4+����c��H+����c��OH�������������䣮
��1������ƽ�ⳣ������������Ũ�ȵ�ϵ������֮�����Է�ӦŨ��ϵ������֮��дƽ�ⳣ���ı���ʽ�������¶ȶ�ƽ���ƶ���Ӱ���жϷ�Ӧ��ƽ�ⳣ���ı仯������v= ![]() �����м��㣻һ��������ת���ʱ��˵��ƽ�������ƶ�����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ����3��ԭ�仯�����ֲ��䣬˵����ƽ��״̬����4����������1mol���ʵ�ϡ�����л���ͨ��1mol NH3����Һ����仯���Բ��ƣ��������Ȼ�泥���ǿ�������Σ�����Ũ�ȵĴ�СΪ��c��Cl������c��NH4+����c��H+����c��OH����������Ũ�ȼ������䣮
�����м��㣻һ��������ת���ʱ��˵��ƽ�������ƶ�����2����ҵ�ϳɰ��ķ�Ӧ�ǿ���ģ�ѡ��500�����ҵĽϸ��¶���ʹ��Ӧ������У������ڻ�ѧƽ��������ƶ���ʹ�ø��¶���Ҫ�ǿ��Ǵ����Ĵ�Ч���Լ���Ӧ���ʵ�֪ʶ����3��ԭ�仯�����ֲ��䣬˵����ƽ��״̬����4����������1mol���ʵ�ϡ�����л���ͨ��1mol NH3����Һ����仯���Բ��ƣ��������Ȼ�泥���ǿ�������Σ�����Ũ�ȵĴ�СΪ��c��Cl������c��NH4+����c��H+����c��OH����������Ũ�ȼ������䣮

 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�����Ŀ�������±������ķ���ʽ���У��жϿո�������ͬ���칹����Ŀ�ǣ� ��
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A.3
B.4
C.5
D.6