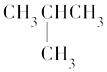题目内容
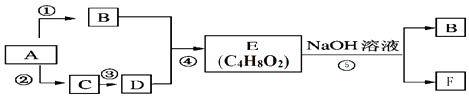
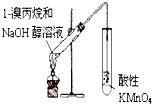
【题目】由乙烯和其他无机原料合成环状化合物E,请在方框内填入合适的化合物的结构简式,并写出A和E的水解方程式. 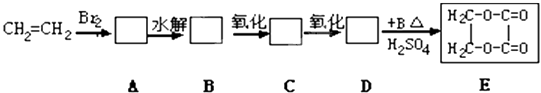
(1)结构简式ABCD
(2)A水解方程式;E水解方程式 .
【答案】
(1)BrCH2CH2Br;HOCH2CH2OH;HOCH2COOH(或HOCH2CHO、OHC﹣CHO、OHC﹣COOH);HOOC﹣COOH
(2)BrCH2CH2Br+2NaOH→HOCH2CH2OH+2NaBr;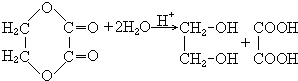
【解析】解:(1)乙烯与溴发生加成,则A为BrCH2CH2Br,水解生成B,则B为HOCH2CH2OH,B氧化生成C,C为HOCH2COOH(或HOCH2CHO、OHC﹣CHO、OHC﹣COOH),C氧化生成D,则D为HOOC﹣COOH,B与D发生酯化反应生成E,所以答案是:BrCH2CH2Br;HOCH2CH2OH;HOCH2COOH(或HOCH2CHO、OHC﹣CHO、OHC﹣COOH);HOOC﹣COOH;(2)A水解方程式为BrCH2CH2Br+2NaOH→HOCH2CH2OH+2NaBr,
E水解反应为 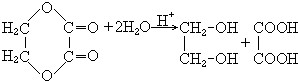 ,
,
所以答案是:BrCH2CH2Br+2NaOH→HOCH2CH2OH+2NaBr; 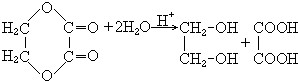 .
.

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案【题目】氮的单质及其化合物性质多样,用途广泛. 完成下列填空.
(1)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2:2NO+2CO ![]() 2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
该反应平衡常数K的表达式为;温度升高,K值(选填“增大”、“减小”、“不变”);前2s内的平均反应速率v(N2)=;若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是 .
(2)工业合成氨的反应温度选择500℃左右的原因是 .
(3)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是 . a.N2、H2、NH3的浓度之比为1:3:2
b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化
d.反应停止,正、逆反应的速率都等于零
(4)常温下向含1mol溶质的稀盐酸中缓缓通入1mol NH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是;在通入NH3的过程中溶液的导电能力(选填“变大”、“变小”、“几乎不变”).