��Ŀ����
18����ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г��������У���ɵ���I��Ԫ���ǵؿ��к�����ߵĽ���Ԫ�أ�K��һ�ֺ���ɫ���壬GΪ���ʣ�������G����J��Һ��Ӧ�õ�M��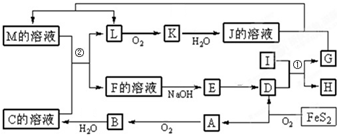
����д���пհף�
��1�������ڱ��У���ɵ���I��Ԫ�������ڱ��е�λ�õ�3���ڢ�A�壮
��2���ڷ�Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��2��
��3��д����Ӧ�ڵ����ӷ���ʽ3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��4����������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч��ˮ��K2FeO4��������أ���ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽFe2O3+3KNO3+4KOH$\frac{\underline{\;����\;}}{\;}$2K2FeO4+3KNO2+2H2O��
���� I���ɵؿ��к������Ľ���Ԫ����ɵĵ��ʣ�ӦΪAl��K��һ�ֺ���ɫ���壬�ж�ΪNO2����JΪHNO3��LΪNO���ɷ�Ӧ4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3+8SO2��A����������Ӧ����B��֪��AΪSO2����DΪFe2O3�����A+O2 ��B֪BΪSO3��CΪH2SO4��I��D��Ӧ����GΪ���ʣ����֪�÷�ӦΪ���ȷ�Ӧ������GΪFe��HΪAl2O3��������G����J��Һ��Ӧ�õ�M��MӦΪFe��NO3��2��M��C��Ӧ��FΪFe��NO3��3��Fe2��SO4��3��F���������Ʒ�Ӧ��EӦΪFe��OH��3��E���ȷֽ��D���ݴ˴��⣮
��� �⣺I���ɵؿ��к������Ľ���Ԫ����ɵĵ��ʣ�ӦΪAl��K��һ�ֺ���ɫ���壬�ж�ΪNO2����JΪHNO3��LΪNO���ɷ�Ӧ4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3+8SO2��A����������Ӧ����B��֪��AΪSO2����DΪFe2O3�����A+O2 ��B֪BΪSO3��CΪH2SO4��I��D��Ӧ����GΪ���ʣ����֪�÷�ӦΪ���ȷ�Ӧ������GΪFe��HΪAl2O3��������G����J��Һ��Ӧ�õ�M��MӦΪFe��NO3��2��M��C��Ӧ��FΪFe��NO3��3��Fe2��SO4��3��F���������Ʒ�Ӧ��EӦΪFe��OH��3��E���ȷֽ��D��
��1��IΪAl�������ڱ��е�λ���ǵ�3���ڢ�A�壬
�ʴ�Ϊ����3���ڢ�A�壻
��2����Ӧ��ΪFe2O3+2Al$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe����Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��2��
�ʴ�Ϊ��1��2��
��3����Ӧ�ڵ����ӷ���ʽΪ 3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
�ʴ�Ϊ��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O��
��4����������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч��ˮ��K2FeO4��������أ���ͬʱ������KNO2��H2O������Ԫ���غ��������ԭ��Ӧ�е��ӵ�ʧ�غ��֪���÷�Ӧ�Ļ�ѧ����ʽΪFe2O3+3KNO3+4KOH$\frac{\underline{\;����\;}}{\;}$2K2FeO4+3KNO2+2H2O��
�ʴ�Ϊ��Fe2O3+3KNO3+4KOH$\frac{\underline{\;����\;}}{\;}$2K2FeO4+3KNO2+2H2O��
���� ���⿼��������ƶϣ���Ŀ�Ѷ��еȣ�����ע�������ʵ��������ַ�����ץס�������ʵ��������ʣ�����ɫ��״̬�ȣ���ȷ���������ʣ����ݿ�ͼѰ�����������ƶϣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | �Զ��ױ� | B�� | ��ϩ | C�� | ��Ȳ | D�� | ������ |
| ��ѧ�� | H-H | H-Cl | H-I | Cl-Cl | Br-Br |
| ����/kJ/mol | 436 | 431 | 299 | 247 | 193 |
| A�� | HCl | B�� | HBr | C�� | H2 | D�� | Br2 |
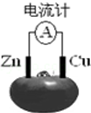
| A�� | п�缫Ϊ��ص����� | |
| B�� | ͭ�缫����������Ӧ | |
| C�� | ����һ��ʱ���пƬ��������� | |
| D�� | ��ع���ʱ��ͭ�缫�����������ɫ |
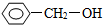 ��ͬ����ǣ�������
��ͬ����ǣ�������| A�� |  | B�� |  | C�� | CH3CH2OH | D�� | HOCH3 |
| A�� | 1mol�л��� �ֱ�����1molNa2CO3��2molNa��3molBr2��4molNaOH��Ӧ �ֱ�����1molNa2CO3��2molNa��3molBr2��4molNaOH��Ӧ | |
| B�� | �л������ ��������Һ���ú��Ծ��й�ѧ���� ��������Һ���ú��Ծ��й�ѧ���� | |
| C�� |  ����ȷ����Ϊ2��3��3��6��6-���-4-�һ����� ����ȷ����Ϊ2��3��3��6��6-���-4-�һ����� | |
| D�� | 2-��-1��3-����ϩ��һ���¶��º�Br2�����ʵ���֮��1��1�����ӳɷ�Ӧ�����ò�����Ҫ������ |
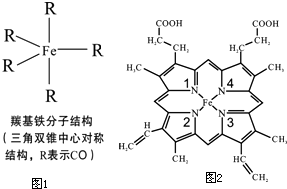 Fe��C��N��O��H������ɶ������ʣ��ش��������⣺
Fe��C��N��O��H������ɶ������ʣ��ش��������⣺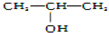
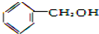
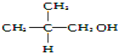
 ��FԪ��ԭ�ӵĵ����Ų�ʽ1s22s22p63s23p5��
��FԪ��ԭ�ӵĵ����Ų�ʽ1s22s22p63s23p5��