题目内容
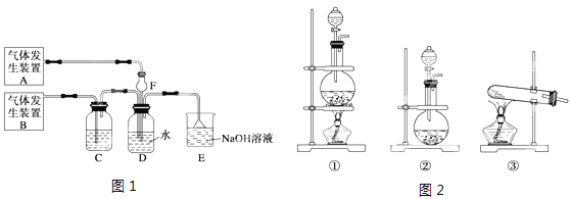
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数。
(1)写出A、B元素的名称 、 。
(2)B位于元素周期表中第 周期第 族。
(3)C的原子结构示意图为 。
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 。
【答案】26.(1)氮、硫 (2)三周期第ⅥA族 (3)![]() (4)NH3+HNO3= NH4NO3
(4)NH3+HNO3= NH4NO3
【解析】试题分析:根据元素周期表,A、B、C为短周期元素,从A、B、C的相对位置看,A、C只能处在第二周期,而B处在第三周期.设A的原子序数为x-1,则C为x+1,B为x+8,则有(x-1)+x+1="x+8" x=8,所以A、B、C的原子序数分别为7、16、9,对应的元素分别为N、S、F。
(1)根据上述推断,A、B元素的名称氮、硫。
(2)根据上述推断,B为S元素,S位于第三周期ⅥA主族。
(3)根据上述推断,C为F,F原子核外有2个电子层,最外层7个电子,原子结构示意图为![]() 。(4)A的气态氢化物NH3与A的最高价氧化物对应水化物为HNO3,两者反应生成硝酸铵,化学方程式为NH3+HNO3= NH4NO3。
。(4)A的气态氢化物NH3与A的最高价氧化物对应水化物为HNO3,两者反应生成硝酸铵,化学方程式为NH3+HNO3= NH4NO3。

【题目】 X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表
元素 | 结构或性质信息 |
X | 其原子最外层电子数是内层电子数的2倍 |
Y | 基态原子最外层电子排布为nsnnpn+1 |
Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
M | 单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
Q | 其与X形成的合金为目前用量最多的金属材料 |
(1)Q元素基态原子的电子排布式是________,Y原子的电子排布图是 。
(2)比较Y元素与氧元素的第一电离能____>____;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是 ,分子中的![]() 键和
键和![]() 键数目之比为_____。
键数目之比为_____。
(3)写出实验室制备M单质的离子方程式 。
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是_____________,其原因是_____________________;
沸点高的是_____________,其原因是_____________________。