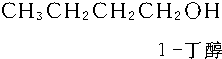题目内容
5.1953年合成出透明如玻璃、坚韧如钢的聚碳酸酯,可作防弹玻璃、防暴警察的护身盾牌、宇航员头盔上的防护眼镜等.其中一种可由含活性氯原子的光气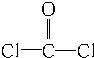 和双酚A:
和双酚A: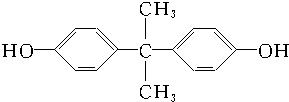 缩聚而成,其反应方程式为
缩聚而成,其反应方程式为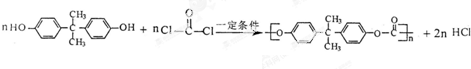 .
.
分析 在一定条件下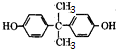 与
与 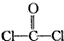 发生缩聚反应生成聚碳酸酯.
发生缩聚反应生成聚碳酸酯.
解答 解:在一定条件下 与
与 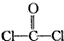 发生缩聚反应生成聚碳酸酯,反应方程式为
发生缩聚反应生成聚碳酸酯,反应方程式为 ,
,
故答案为: .
.
点评 本题主要考查了有机物的结构与性质,难度不大,熟练运用官能团的性质来书写方程式.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案
相关题目
15.打雷及雷雨后,空气中的部分氮气最后转化成植物,能从土壤中吸收的是( )
| A. | N2 | B. | NO | C. | NH4+ | D. | 硝酸盐中的NO3- |
13.某烃的一个分子中所含电子总数比原子个数多30个,既能发生取代反应,又能发生加成反应,此烃是下列中的( )
| A. | 1-丁烯 | B. | 二甲苯 | C. | 苯 | D. | 环己烷 |
20.下列对高分子材料的研究方向,不正确的一项是( )
| A. | 使高分子材料具有仿生能力 | |
| B. | 使高分子材料向功能材料方向发展 | |
| C. | 使高分子材料越来越牢固,难分解 | |
| D. | 使农用薄膜能够选择性地透过某种植物所需要的特定波长的光 |
10.下列反应中有机物被还原的是( )
① +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl3+2H2O
+3FeCl3+2H2O
②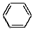 +3H2$→_{△}^{催化剂}$
+3H2$→_{△}^{催化剂}$
③2CH2═CH2+O2→2CH3CHO
④CH3CH2Cl+H2O$→_{△}^{NaOH}$ CH3CH2OH+HCl.
①
 +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl3+2H2O
+3FeCl3+2H2O②
 +3H2$→_{△}^{催化剂}$
+3H2$→_{△}^{催化剂}$
③2CH2═CH2+O2→2CH3CHO
④CH3CH2Cl+H2O$→_{△}^{NaOH}$ CH3CH2OH+HCl.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
14. 一氧化碳是一种用途十分广泛的化工基础原料.
一氧化碳是一种用途十分广泛的化工基础原料.
(1)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g);△H1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g);△H2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g);△H3=-296.0kJ•mol-1
请写出CO除SO2的热化学方程式2CO(g)+SO2(g)=S(s)+2CO2(g);△H=-270 kJ•mol-1.
(2)工业上一般采用CO与H2在一定条件下反应合成甲醇,反应为:CO(g)+2H2(g)?CH3OH(g).在不同温度下的化学平衡常数(K)如下表:
①某温度下,将2molCO(g)和6molH2(g)充入2L密闭容器中,充分反应后,达到平衡时测得c(CO)=0.5mol/L,则CO(g)的转化率为50%,此时的温度为300℃.
②在恒容条件下,要提高CO(g)的转化率,可以采取的措施有DE(填字母序号).
A、升高温度 B、加入催化剂 C、增加CO(g)的浓度
D、充入H2(g)加压E、分离出甲醇 F、充入稀有气体加压
③实际生产过程中,合成气要进行循环,其目的是提高原料利用率.
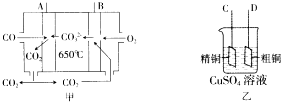
(3)如图甲是--碳酸盐燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质;图乙是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.
请回答下列问题:
①写出A极发生的电极反应式CO-2e-+CO32-=2CO2.
②要进行粗铜的精炼实验时,则B极应与D极(填“C”或“D”)相连.
③当消耗2.24L(标准状况下) CO时,粗铜电极理论上减少铜的质量小于(填“大于”、“等于”或“小于”)6.4g.
 一氧化碳是一种用途十分广泛的化工基础原料.
一氧化碳是一种用途十分广泛的化工基础原料.(1)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g);△H1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g);△H2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g);△H3=-296.0kJ•mol-1
请写出CO除SO2的热化学方程式2CO(g)+SO2(g)=S(s)+2CO2(g);△H=-270 kJ•mol-1.
(2)工业上一般采用CO与H2在一定条件下反应合成甲醇,反应为:CO(g)+2H2(g)?CH3OH(g).在不同温度下的化学平衡常数(K)如下表:
| 温度 | 250℃ | 300℃ | 350℃ |
| A | 2.041 | 0.250 | 0.012 |
②在恒容条件下,要提高CO(g)的转化率,可以采取的措施有DE(填字母序号).
A、升高温度 B、加入催化剂 C、增加CO(g)的浓度
D、充入H2(g)加压E、分离出甲醇 F、充入稀有气体加压
③实际生产过程中,合成气要进行循环,其目的是提高原料利用率.
(3)如图甲是--碳酸盐燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质;图乙是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.
请回答下列问题:
①写出A极发生的电极反应式CO-2e-+CO32-=2CO2.
②要进行粗铜的精炼实验时,则B极应与D极(填“C”或“D”)相连.
③当消耗2.24L(标准状况下) CO时,粗铜电极理论上减少铜的质量小于(填“大于”、“等于”或“小于”)6.4g.
15.H2和O2的混合气体,在120℃和1.01×105Pa下体积为aL,点燃使其反应后恢复至原条件,其体积变为bL,则原混合气体中O2为( )
| A. | b L | B. | (b-a)L | C. | (2a-b)L | D. | (2b-a)L |
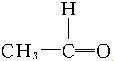 +
+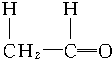 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$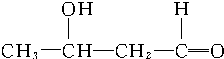
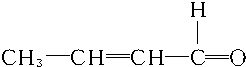 +2H2$→_{△}^{催化剂}$
+2H2$→_{△}^{催化剂}$