��Ŀ����
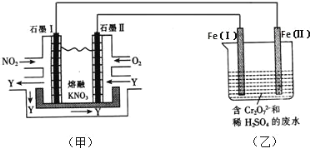
����Ŀ���ռ�ʵ�������칬һ�����Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ� ��

A. ����0.8mol����ת��ʱ��b������4.48LO2
B. Ϊ�����ӵ����Կ��Խ���������е�ˮ��ΪNaOH��Һ
C. d���Ϸ����ĵ缫��Ӧ�ǣ�2H+ +2e��=H2
D. c���Ͻ���������Ӧ��A���е�H+����ͨ����Ĥ����B
���𰸡�B
��������
A.û��ָ�������������¶Ⱥ�ѹǿ������������������A�����
B.���NaOH��Һ��ʵ���ǵ��ˮ�����Խ���ߵĵ��ˮװ���е�ˮ��ΪNaOH��Һ��������Һ�����ӵ�Ũ�ȣ���ǿ�����ԣ�B����ȷ��
C.a�缫Ϊ������a�缫�ϲ�����������������d�缫�����ĵ缫��Ӧ�ǣ�H2-2e-=2H+��C�����
D.b�缫Ϊ������b���ϲ���������YΪ������c����������������ԭ��Ӧ��O2+4e-+4H+=2H2O��c��Ϊȼ�ϵ�ص�������d��Ϊȼ�ϵ�صĸ�����B���е�H+ͨ����Ĥ����A�أ�D�����
���Դ�ѡ��B�

����Ŀ�������̼����(Na2CS3)������ɱ��������������ijС�����ʵ��̽�������̼���Ƶ����ʲ��ⶨ����Һ��Ũ�ȡ�
ʵ��1��̽��Na2CS3������
���� | ���������� |
�� | ȡ����Na2CS3������������ˮ���Ƴ���Һ���ֳ����ȷ� |
�� | ������һ����Һ�еμӼ��η�̪��Һ����Һ���ɫ |
�� | ����һ����Һ�еμ�����KMnO4��Һ����ɫ��ȥ |
��1��H2CS3��________�ᣨ�ǿ������������
��2����֪����۵�����������SO42��,д���÷�Ӧ�����ӷ���ʽ______
��3��ijͬѧȡ�����������Һ���Թ��У��μ��������ᡢBaCl2��Һ������ɫ����������Ϊͨ���ⶨ�����İ�ɫ�����������������ʵ������Na2CS3���������Ƿ�ͬ�����Ĺ۵㲢˵������______��
ʵ��2���ⶨNa2CS3��Һ��Ũ��

����ͼ��ʾ���Ӻ�װ�ã�ȡ100mLNa2CS3��Һ����������ƿ�У�������d�Ļ�������������2.0mol/LϡH2SO4���رջ�����
��֪��Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S����CS2��H2S���ж���CS2������ˮ���е�46�棬��CO2ijЩ�������ƣ���NaOH��������Na2COS2��H2O��
��4��ʢ����ˮCaCl2��������������______��B�з�����Ӧ�����ӷ���ʽ��______��
��5����Ӧ���������k���ٻ���ͨ����N2һ��ʱ�䣬��Ŀ����______��
��6��Ϊ�˼���Na2CS3��Һ��Ũ�ȣ���B�л������й��ˡ�ϴ�ӡ�������أ���19.2g���壬��A��Na2CS3�����ʵ���Ũ��Ϊ______��
��7����������ʵ�鷽����������ͨ���ⶨC����Һ����������ֵ������Na2CS3��Һ��Ũ�ȣ�����Ӧ������ͨ��N2��Ϊͨ�ȿ���������ֵ______���ƫ�ߡ�����ƫ�͡�����Ӱ�족����