题目内容
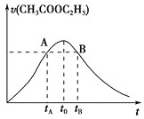
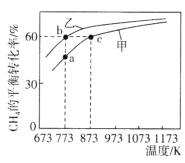
【题目】甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2,乙中充入1molCH4和nmolCO2,在催化剂存在下发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
A.该反应的正反应是吸热反应
B.773K时,该反应的平衡常数小于12.96
C.H2的体积分数:![]()
D.873K时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,平衡不发生移动
【答案】AB
【解析】
A.温度升高,CH4的平衡转化率增大,说明温度升高有利于反应正向进行,则正反应为吸热反应,故A正确;
B.873K时,c点CH4的平衡转化率为60%,列“三段式”:

则K(c)=![]() =12.96,温度升高,CH4的平衡转化率增大,平衡正向移动,平衡常数增大,则773K时该反应的平衡常数小于12.96,故B正确;
=12.96,温度升高,CH4的平衡转化率增大,平衡正向移动,平衡常数增大,则773K时该反应的平衡常数小于12.96,故B正确;
C.根据图像,相同温度下乙中甲烷的平衡转化率大于甲中,则n>1,b、c点甲烷的平衡转化率相等,则两点平衡时体系中CH4、CO、H2物质的量分别相等,但b中CO2物质的量大于c中,则H2的体积分数:![]() ,故C错误;
,故C错误;
D.873K时,甲容器中甲烷的转化率为60%,列三段式:
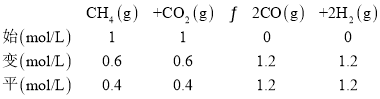
平衡常数K=![]() =12.96,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,Qc=
=12.96,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,Qc=![]() =51.84>K=12.96,平衡逆向移动,故D错误;
=51.84>K=12.96,平衡逆向移动,故D错误;
答案选AB。

【题目】在钯基催化剂表面上,甲醇制氢的反应历程如图所示,其中吸附在钯催化剂表面上的物种用*标注。
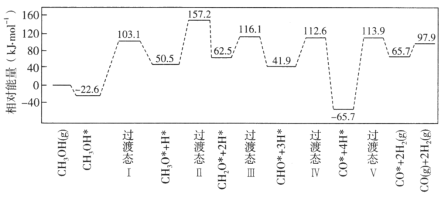
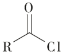
(1)![]() 的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
的△H=_____________kJ·mol-1;该历程中最大能垒(活化能)E正=____________kJ·mol-1,写出该步骤的化学方程式_________________。
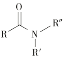
(2)在一定温度下,CO和H2混合气体发生反应:![]() ,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,
,反应速率υ=υ正-υ逆=k正c(CO)·c2(H2)-k逆c(CH3OH),k正、k逆分别为正、逆反应速率常数。达到平衡后,若加入高效催化剂,![]() 将___________(填“增大”、“减小”或“不变”);若升高温度,
将___________(填“增大”、“减小”或“不变”);若升高温度,![]() 将____________(填“增大”、“减小”或“不变”)。
将____________(填“增大”、“减小”或“不变”)。
(3)353K时,在刚性容器中充入CH3OH(g),发生反应:![]() 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:
t/min | 0 | 5 | 10 | 15 | 20 | ∞ |
p/kPa | 101.2 | 107.4 | 112.6 | 116.4 | 118.6 | 121.2 |
①若升高反应温度至373K,则CH3OH(g)分解后体系压强p∞(373K)___________121.2kPa(填“大于”、“等于”或“小于”),原因是________________________。
②353K时,该反应的平衡常数KP=__________(kPa)2(KP为以分压表示的平衡常数,计算结果保留1位小数)。