题目内容
【题目】CH3COOH、H2SO3是中学化学中常见的弱酸,请回答下列问题:
(1)常温下,下列叙述能证明CH3COOH为弱酸是_________。
a. CH3COONa 溶液的pH大于7;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,PH > 2
(2)常温下,向0.1 mol·L-1 CH3COOH溶液中加蒸馏水稀释,稀释后,下列各量增大的是_________:
a.![]() b.
b.![]() c.c(OH-)
c.c(OH-)
(3)将浓度均为0.1mol/LCH3COOH和CH3COONa溶液等体积混合,测得混合液中c(CH3COO-)>c(Na+),则下列关系式中正确的是(_____)
A.c(H+) > c(OH-) B.c(H+) < c(OH-)
C.c(CH3COOH) > c(CH3COO-) D.c(CH3COOH) + c(CH3COO-)=0.1mol/L
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液呈_______(填“酸性”,“中性”或“碱性”),原因是 _______________(用离子方程式表示)。若将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+) ___________c(CH3COO-) (填“ >” 或“=”或“<” )。
(5)25℃时,H2SO3的电离常数Ka1=1×10-2mol/L,Ka2=6×10-3mol/L,则该温度下NaHSO3的水解平衡常数Kh=__________mol/L。
【答案】acd c AD 碱性 CH3COO- + H2O ![]() OH- + CH3COOH 酸性 < 10-12
OH- + CH3COOH 酸性 < 10-12
【解析】
(1)a.CH3COONa 溶液的pH大于7,则醋酸根离子水解使溶液呈碱性;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气,与酸性的强弱无关,酸物质的量相等,产生的氢气的物质的量相等;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多;
d.0.01mol/L的CH3COOH溶液,pH > 2,说明醋酸中含有未电离的分子;
(2)a.![]() =K,K只与温度有关,温度未变,K不变;
=K,K只与温度有关,温度未变,K不变;
b.![]() =
=![]() ,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小;
,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小;
c. 加水稀释酸性减弱,c(H+)减小,Kw不变,则c(OH-)增大;
(3)A.根据溶液呈电中性,c(CH3COO-)+ c(OH-)=c(Na+)+c(H+);
C.由于c(H+) >c(OH-),则醋酸的电离程度大于醋酸根离子的水解程度;
D.根据物料守恒,c(CH3COOH) + c(CH3COO-)=0.1mol/L;
(4)醋酸钠为强碱弱酸盐,醋酸根离子水解,则溶液呈碱性;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;
(5)根据Kh= 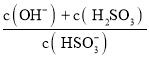 =
=![]() 计算。
计算。
(1)a.CH3COONa 溶液的pH大于7,则醋酸根离子水解使溶液呈碱性,说明醋酸为弱酸,符合题意,a正确;
b.相同体积相同浓度的盐酸和醋酸溶液,分别与足量锌粉反应,放出相同体积的氢气,与酸性的强弱无关,酸物质的量相等,产生的氢气的物质的量相等,与题意不符,b错误;
c.相同体积、相同pH的盐酸和醋酸,醋酸中和NaOH的物质的量多,说明醋酸中含有未电离的分子,醋酸为弱酸,符合题意,c正确;
d.0.01mol/L的CH3COOH溶液,pH > 2,说明醋酸中含有未电离的分子,醋酸为弱酸,符合题意,d正确;
答案为acd。
(2)a.![]() =K,K只与温度有关,温度未变,K不变,与题意不符,a错误;
=K,K只与温度有关,温度未变,K不变,与题意不符,a错误;
b.![]() =
=![]() ,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小,与题意不符,b错误;
,加水稀释酸性减弱,c(H+)减小,K不变,其比值减小,与题意不符,b错误;
c. 加水稀释酸性减弱,c(H+)减小,Kw不变,则c(OH-)增大,符合题意,c正确;
答案为c。
(3)A.根据溶液呈电中性,c(CH3COO-)+ c(OH-)=c(Na+)+c(H+),已知c(CH3COO-)>c(Na+),则 c(H+)> c(OH-) ,A正确;
B.A项解析可知c(H+) >c(OH-),B错误;
C.由于c(H+) >c(OH-),则醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COOH)< c(CH3COO-),C错误;
D.根据物料守恒,c(CH3COOH) + c(CH3COO-)=0.1mol/L,D正确;
答案为AD。
(4)若等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,生成的物质醋酸钠,为强碱弱酸盐,醋酸根离子水解,则溶液呈碱性;水解的离子方程式为CH3COO- + H2O ![]() OH- + CH3COOH;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;溶液中c(Na+) <c(CH3COO-);
OH- + CH3COOH;pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合,醋酸电离出的氢离子的物质的量与NaOH电离出的氢氧根离子的物质的量相等,但醋酸还有未电离的分子,其电离导致溶液呈酸性;溶液中c(Na+) <c(CH3COO-);
(5)HSO3- + H2O ![]() OH- + H2SO3,则Kh=
OH- + H2SO3,则Kh= 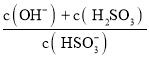 =
=![]() =10-12 mol/L。
=10-12 mol/L。

【题目】含氮化合物在化学工业中有着重要的应用,回答下列问题:
(1)一定条件下,硝酸铵加热分解得到的产物只有N2O和H2O。250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的平衡常数表达式为K=___________;若有1mol硝酸铵完全分解,则转移电子的数目为___________(设NA为阿伏加德罗常数的值)。
(2)硝基苯甲酸乙酯在碱性条件下发生反应:O2NC6H4COOC2H5+OH-![]() O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.80mol·L-1,T℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
t/s | 0 | 60 | 90 | 120 | 160 | 260 | 300 | 360 | 400 |
a/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
①该反应在60~90s与90~120s内的平均反应速率分别约为___________,___________;比较两者大小可得出的结论是______________________。
②计算T℃时该反应的平衡常数为______________________。
③为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可以采取的措施为______________________(写出一条即可)。
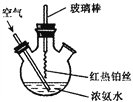
【题目】氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间隙法”制取,反应原理、实验装置图(加热装置都已略去)如下:![]()
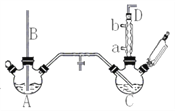
已知:氯苯为无色液体,沸点132.2℃.
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是___________,冷凝管中冷水应从______(填“a”或“b”) 处通入。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯.
①对C加热的方法是_________(填序号)
a.酒精灯加热 b.油浴加热 c.水浴加热
②D出口的气体成分有HCl、________和________;
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本.写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:_____________________;_________________;(写两个即可)
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是________________;
(5)工业生产中苯的流失情况如下:
项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
则lt苯可制得成品为________________t(只要求列式)。