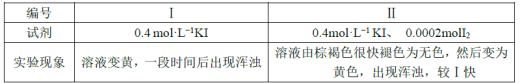
��Ŀ����
����Ŀ��ʵ�����Ʊ�1��2����������ķ�Ӧԭ�����£�CH3CH2OH![]() CH2=CH2��CH2=CH2+Br2��CH2BrCH2Br
CH2=CH2��CH2=CH2+Br2��CH2BrCH2Br
���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������140����ˮ�������ѣ�Ũ������Ҵ�����ΪCO2�ȡ�������������������Ҵ��Ʊ�1��2�����������װ����ͼ��ʾ��
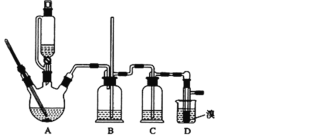
�ش��������⣺
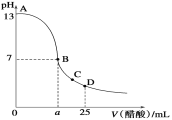
��1���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ����__��
a.������Ӧ b.�ӿ췴Ӧ�ٶ� c.��ֹ�Ҵ��ӷ� d.���ٸ�������������
��2����װ��C��Ӧ����__��������ţ���Ŀ�������շ�Ӧ�п������ɵ��������塣
a.ˮ b.Ũ���� c.����������Һ d.����̼��������Һ
��3���жϸ��Ʊ���Ӧ�Ѿ��������������__��
��4����1��2����������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ��__�㣨������������������
��5����������������δ��Ӧ��Br2�������___ϴ�ӳ�ȥ������ţ�
a.ˮ b.����������Һ c.�⻯����Һ d.�Ҵ�
��6�������������������������ѣ�����___�ķ�����ȥ��
��7����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ����__�����ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ����___��
���𰸡�d c �����ɫ��ȫ��ȥ �� b ���� ����������ӷ� ��Ʒ1��2����������ķе�ͣ�������ȴ�����̶���������
��������
����ʵ��ԭ����װ��AΪ��ȡ��ϩ��װ�ã���Ӧʱ�и���Ӧ���ڣ���ϩ�����д��ڶ�����̼��������������ʣ�װ��B�����г��������ܣ�����������ͨ������ȫƿ�����ã���ֹ������װ��CΪ���������������ʣ�ʢ��NaOH��Һ��װ��DΪ��ϩ���巴Ӧ����1��2���������顣
��1���Ҵ���Ũ����140���������£�������������ˮ���������ѣ���ʵ����Ҫ�������µ�170�棬�Լ������ѵ����ɣ���Ϊd��
��2��Ũ�������ǿ�����ԣ����Ҵ������ɶ�����̼����������ԭ�ɶ�����������̼�����������ܺ�����������Һ��Ӧ����Ϊc��
��3����ϩ����ˮ�����ӳɷ�Ӧ����1��2-�������飬1��2-��������Ϊ��ɫ����Ӧ����ʱ����ˮ��Һ��ɫ����Ϊ�����ɫ��ȫ��ȥ��
��4��1��2-���������ˮ�����ܣ�1��2-���������ܶȱ�ˮ���ú������²㣻
��5��������NaOH��Ӧ����1��2-�������鲻��NaOH��Ӧ���Ҳ�����NaOH��Һ��������������δ��Ӧ��Br2����������������Һϴ�ӳ�ȥ����Ϊb��
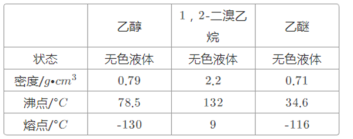
��6��1��2-�������������ѵķе㲻ͬ�����߾�Ϊ�л�����ܣ�������ķ��������Ƿ��룬��Ϊ����
��7�����ڳ����£��ӷ�����ϩ���巴Ӧʱ���ȣ�����ӷ�����ȴ�ɱ�����Ĵ����ӷ�����1��2-������������̵�9���ϵͣ�������ȴ��ʹ�����̶�ʹ��·������

����Ŀ��(1) CO2��NH3��Ӧ�ɺϳɻ������ء���֪��
��2NH3(g)+CO2(g) = NH2CO2NH4(s) ��H= -159.5kJmol-1
��NH2CO2NH4(s) = CO(NH2)2(s)+H2O(g) ��H= +116.5kJmol-1
��H2O(l) = H2O(g) ��H= +44.0kJmol-1
д��CO2��NH3�ϳ�����[CO(NH2)2]��Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽ_____
(2)ʹCl2��H2O(g)ͨ�����ȵ�̿�㣬����HCl��CO2����1mol Cl2���뷴Ӧʱ�ͷ�145kJ��������д�������Ӧ�淴Ӧ���Ȼ�ѧ����ʽ��______ ��
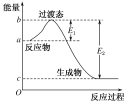
(3)��ͼ��1mol NO2(g)��1mol CO(g)��Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��________(��������������С����������������ͬ)����H�ı仯��________��
(4)��֪H��H����N��N����N-H���ļ������±���ʾ��
��ѧ�� | H-H | N��N | N-H |
����/(kJ��mol-1) | 436 | 946 | 391 |
��ӦN2(g)��3H2(g)=2NH3(g)�� ��H��________��