题目内容
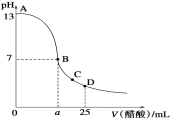
【题目】25℃时,在25 mL 0.1 mol·L-1的NaOH溶液中,逐滴加入0.2 mol·L-1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析正确的是( )
A. 该滴定过程应该选择甲基橙作为指示剂
B. B点的横坐标a=12.5
C. 水的电离程度:D > C > B
D. D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+)
【答案】D
【解析】A. 该滴定过程为弱酸滴定强碱,滴定终点是溶液显碱性;B、a=12.5时,氢氧化钠和醋酸的物质的量之比1:1,恰好反应生成CH3COONa,CH3COONa为强碱弱酸盐,溶液显碱性;C. 根据滴定原理可知,B、C、D均为醋酸过量,水解的电离均受到抑制;D、在D点时,氢氧化钠溶液和醋酸溶液反应后剩余醋酸,溶液的组成为等浓度的醋酸和醋酸钠的混合物;据此分析判断。
A. 用强碱滴定弱酸,滴定终点是溶液显碱性,应该选用酚酞作为指示剂,故A错误;B、当a=12.5时,氢氧化钠和醋酸的物质的量之比1:1,恰好反应生成CH3COONa,CH3COONa为强碱弱酸盐,溶液显碱性,与pH=7不符,故B错误;C. B点时溶液显中性,则醋酸过量,C、D溶液显酸性,醋酸过量更多,水的电离受到抑制水的电离程度:D<C<B,故C错误;D、在D点时,反应后醋酸剩余,溶液的组成为等浓度的醋酸和醋酸钠的混合物,根据物料守恒,此时c(CH3COO-)+c(CH3COOH)=2c(Na+),故D正确;故选D。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO |
阳离子 | Al3+、Fe3+、Mg2+、NH、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是___,ab段发生反应的离子是______________,bc段发生反应的离子方程式为______________。
(2)若Y是NaOH溶液,则X中一定含有的离子是___________________。ab段反应的离子方程式为_______________________________________。