��Ŀ����
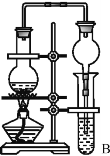
����Ŀ���������Ƭ�Ķ�Ӱ�����У�δ�ع���廯��(AgBr)�������������(Na2S2O3)�ܽ⣬��Ӧ����Na3[Ag(S2O3)2]���ڷ϶�ӰҺ�м���Na2SʹNa3[Ag(S2O3)2]�е���ת��ΪAg2S����ʹ��ӰҺ��������Ag2S�ڸ�����ת��ΪAg���ʹﵽ�˻�������Ŀ�ġ�
(1)ͭ����������Ԫ�����ڱ���λ��ͬһ���������ڣ���̬��ԭ�ӵ����������Ų�ʽΪ _______��
(2)Na��O��S�����Ӱ뾶�ɴ�С��˳��Ϊ______________________��
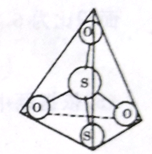
(3)S2O32-���ӽṹ��ͼ��ʾ����������ԭ�ӵ��ӻ��������Ϊ_______________________��
(4)д��AgBr ����Na2S2O3��Һ�����ӷ�Ӧ����ʽ______________��Na3[Ag(S2O3)2]�д��ڵ������������Ӽ������ۼ���______________��
(5)�ڿ���������Ag2S����Ag��SO2��SO2 ��������ԭ�ӵļ۲���Ӷ���Ϊ_________������ӿռ乹��Ϊ______________�� SO2������ˮ��ԭ����________________________________��
(6)���������Ѿ��ж��ַ������ⶨ�����ӵ�������X�������䷨�������е�һ�֣�ͨ���Խ����X ��������ͼ��ķ��������Եó�����ľ�������������������(��ͭ�ľ�������)������ԭ�ӵİ뾶Ϊam������ܶ�Ϊ��g��cm-3�����Ħ������ΪMg��mol -1����ͨ����Щ�����г����㰢���ӵ���������ʽ______________________________��
���𰸡� 5s1 S2- O2- Na+ sp3 AgBr+2S2O32-==[Ag(S2O3)2]3-+Br- ��λ�� 3 V�� ������������ԭ����SO2��ˮ��Ϊ���Է��ӣ���SO2��ˮ��Ӧ ![]()
��������(1). ͭ����������Ԫ�����ڱ���λ��ͬһ���������ڣ���̬ͭԭ�ӵ����������Ų�ʽΪ4s1�����̬��ԭ�ӵ����������Ų�ʽΪ5s1���ʴ�Ϊ��5s1��
(2). ���Ӳ���Խ�࣬���Ӱ뾶Խ��������Ų���ͬ�����ӣ�ԭ������Խ�����Ӱ뾶ԽС����Na��O��S�����Ӱ뾶�ɴ�С��˳��ΪS2-�� O2- ��Na+���ʴ�Ϊ��S2- O2- Na+��
(3). ��S2O32-���ӽṹʾ��ͼ��֪����������ԭ���γ�4���Ҽ�����������ԭ�ӵ��ӻ��������Ϊsp3���ʴ�Ϊ��sp3��
(4). AgBr��Na2S2O3��Һ��Ӧ����Na3[Ag(S2O3)2]��NaBr���÷�Ӧ�����ӷ�Ӧ����ʽΪAgBr+2S2O32-=[Ag(S2O3)2]3-+Br-��Na3[Ag(S2O3)2]�д��ڵ������������Ӽ������ۼ�����λ�����ʴ�Ϊ��AgBr+2S2O32-=[Ag(S2O3)2]3-+Br-����λ����
(5). SO2 ��������ԭ�ӵļ۲���Ӷ���Ϊ��2+![]() =2+1=3����SO2 �����к���1���µ��Ӷԣ���������ӿռ乹��ΪV�Σ���SO2��ˮ��Ϊ���Է��ӣ���SO2���Ժ�ˮ������Ӧ������SO2������ˮ���ʴ�Ϊ��3��V�Σ�������������ԭ����SO2��ˮ��Ϊ���Է��ӣ���SO2��ˮ��Ӧ��
=2+1=3����SO2 �����к���1���µ��Ӷԣ���������ӿռ乹��ΪV�Σ���SO2��ˮ��Ϊ���Է��ӣ���SO2���Ժ�ˮ������Ӧ������SO2������ˮ���ʴ�Ϊ��3��V�Σ�������������ԭ����SO2��ˮ��Ϊ���Է��ӣ���SO2��ˮ��Ӧ��
(6). ����ľ�����������������������1�������к��н�ԭ�ӵĸ���Ϊ8��![]() +6��
+6��![]() =4����ԭ�ӵİ뾶Ϊa��102cm������ı߳�Ϊ
=4����ԭ�ӵİ뾶Ϊa��102cm������ı߳�Ϊ![]() cm�����Խ���ܶ�Ϊ��g��cm-3 =
cm�����Խ���ܶ�Ϊ��g��cm-3 =![]() �����
�����![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��

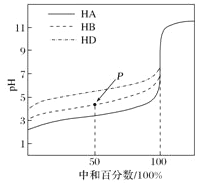
����Ŀ����1��X��Y��Z����Һ��Ľ���pH��ͼ�������ж���ȷ����___________��

A��Xһ�������ǿ����������Һ B��Yһ����90��ʱ�Ĵ�ˮ
C��YҺ��һ�������� D��Z������Na2SiO3��Һ
��2�����ʵ���Ũ����ͬ��������Һ����NH4Cl�ڰ�ˮ��NH4HSO4��c(NH4+)��С˳����ȷ����___________��
A����>��>�� B����>��>�� C����>��>�� D����>��>��
��3���Ƚ����(ѡ�>"�� <"��"=����
�ٳ�����������Һ��a��pH=4���� b��pH=4NH4Cl��Һ������ˮ�ĵ���̶ȴ�С��a____b��
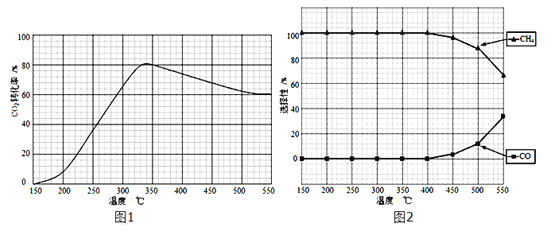
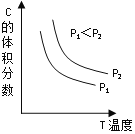
����֪ij���淴ӦaA(g)+bB(g)![]() cC(g)+dD(g)����������������ʱ��C������������¶ȣ�T����ѹǿ��P���Ĺ�ϵ����ͼ��ʾ����Ӧ���������Ļ�ѧ������֮�ͣ�a+b____c+d��
cC(g)+dD(g)����������������ʱ��C������������¶ȣ�T����ѹǿ��P���Ĺ�ϵ����ͼ��ʾ����Ӧ���������Ļ�ѧ������֮�ͣ�a+b____c+d��
��4����һ��������ܱ������м���1molCO2��1mol H2���������»�ѧ��Ӧ��CO2(g)+ H2(g) ![]() CO(g)+H2O(g) ���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
CO(g)+H2O(g) ���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
T(��) | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=__________________________��
�ڷ�ӦΪ___________��Ӧ������ȡ����ȡ�����
��800�棬�������ڳ���lmolCO2��lmolH2��lmol CO��lmolH2O���˿̷�Ӧ��v��_______v�������"������=����