题目内容
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
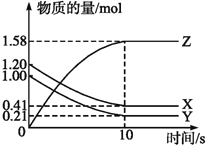
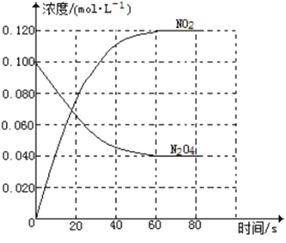
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1反应的平衡常数K1为___________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K2___________
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反应”)方向移动,判断理由是___________。
【答案】大于 0.001 0.36 mol·L—1 大于 反应正方向吸热,反应向吸热方向进行,故温度升高 平衡时,c(NO2)=0.120 mol·L—1+0.002 mol·L—1·s—1×10s×2=0.160mol·L—1
c(N2O4)=0.040 mol·L—1—0.002 mol·L—1·s—1×10s=0.02 mol·L—1
K2=0.160mol·L—1)2/0.020mol·L—1=1.3mol·L—1 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】
(1)根据题意知,随温度升高,混合气体的颜色变深,二氧化氮的浓度增大,说明平衡向正反应方向移动;当其他条件不变时,升高温度,平衡向吸热反应方向移动,说明正反应为吸热反应,故△H大于0。根据题给图像知,0-60s时段,N2O4的物质的量浓度变化为0.060 mol·L-1,根据公式v=△c/△t计算,v (N2O4)= 0.060 mol·L-1/60s=0.001 mol·L-1·s-1;分析题给图像知,二氧化氮的平衡浓度为0.120 mol·L-1,四氧化二氮的平衡浓度为0.040 mol·L-1,K1= [NO2]2/[N2O4]=0.36 mol·L-1;
(2)①根据题意知,改变反应温度为T后,c(N2O4)以0.0020 molL-1s-1的平均速率降低,即平衡向正反应方向移动,又反应正方向吸热,反应向吸热方向进行,故为温度升高,T大于1000C,答案为:大于;反应正方向吸热,反应向吸热方向进行,故温度升高;
②根据题意知,平衡时,c(NO2)=0.120 mol·L-1+0.002 mol·L-1·s-1×10s×2=0.160mol·L-1,c(N2O4)=0.040 mol·L-1-0.002 mol·L-1·s-1×10s=0.02 mol·L-1,K2=(0.160mol·L-1)2/0.020mol·L-1=1.3mol·L-1;
(3)温度为T时,反应达平衡,将反应容器的体积减小一半,即增大压强,当其他条件不变时,增大压强,平衡向气体物质平衡向气体物质系数减小的方向移动,即向逆反应方向移动,答案为:逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动。

 阅读快车系列答案
阅读快车系列答案