题目内容
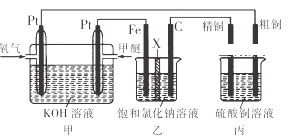
【题目】一种新型污水处理装置模拟细胞内生物电的产生过程,可将酸性有机废水的化学能直接转化为电能。下列说法中不正确的是
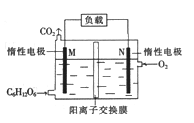
A. M极作负极,发生氧化反应
B. 电子流向:M→负载→N→电解质溶液→M
C. N极的电极反应:O2+4H++4e-=2H2O
D. 当N极消耗5.6L(标况下)气体时,最多有NA个H+通过阳离子交换膜
【答案】B
【解析】
本题考查了原电池的原理和电解原理的应用,注意把握电极的判断方法和电子的流向,侧重于考查学生的分析能力和对基础知识的应用能力。
A. M极加入有机物,有机物变成二氧化碳,发生氧化反应,说明M作负极,故正确;B. M为负极,N为正极,所以电子流向:M→负载→N,电子只能通过导线不能通过溶液,故错误;C. N极为正极,氧气在正极上得到电子,电极反应:O2+4H++4e-=2H2O,故正确;D. 当N极消耗5.6L(标况下)气体基5.6/22.4=0.25mol氧气时,转移0.25×4=1mol电子,所以最多有NA个H+通过阳离子交换膜,故正确。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】一定温度下,在4个体积均为 1.0 L的恒容密闭容器中反应2SO2(g)+O2 (g)![]() 2SO3(g) 达到平衡。
2SO3(g) 达到平衡。
下列说法正确的是
容器 | 温度/K | 物质的起始浓度/moI/L | 物质的平衡浓度moI/L | O2或SO3平衡转化率 | ||
c(SO2) | c(O2) | c(SO3) | c(SO3) | |||
Ⅰ | 723 | 0.2 | 0.2 | 0 | 0.04 | α1 |
Ⅱ | 723 | 0 | 0.1 | 0.2 | α2 | |
Ⅲ | 723 | 0.4 | 0.4 | 0 | α3 | |
IV | 823 | 0 | 0.1 | 0.2 | α4 | |
A. 达到平衡时, α1+α2=1
B. 达到平衡时,容器中的压强:PⅠ>PIV
C. 达到平衡时,逆反应速率容器IV中比容器Ⅰ中的大
D. 达平衡后,再向容器Ⅰ中充入0.16 mol SO2、0.04 mol SO3,则此时反应向逆反应方向进行