题目内容
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 5.6g铁与足量稀硫酸反应转移的电子数为0.3NA | |
| B. | 标准状况下,11.2L水中含有分子的数目为0.5NA | |
| C. | 500 mL 0.2 mol•L-1 CaCl2溶液中氯离子数目为 0.1NA | |
| D. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
分析 A.铁与稀硫酸反应生成硫酸亚铁,0.1mol铁与稀硫酸完全反应转移了0.2mol电子;
B.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算;
C.根据n=cV计算出氯化钙的物质的量,再根据氯化钙的化学式组成计算出含有氯离子的物质的量及数目;
D.氧气和臭氧分子中都只含有氧元素,1.6g二者的混合物中含有1.6g氧原子,含有0.1mol氧原子.
解答 解:A.5.6g铁的物质的量为:$\frac{5.6g}{56g/mol}$=0.1mol,0.1mol铁与足量稀硫酸反应生成0.1mol硫酸亚铁,转移了0.2mol电子,反应转移的电子数为0.2NA,故A错误;
B.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算11.2L水的物质的量,故B错误;
C.500 mL 0.2 mol•L-1 CaCl2溶液中含有溶质氯化钙的物质的量为0.1mol,0.1mol氯化钙中含有0.2mol氯离子,含有氯离子数目为0.2NA,故C错误;
D.1.6g由氧气和臭氧组成的混合物中含有1.6g氧原子,含有氧原子的物质的量为:$\frac{1.6g}{16g/mol}$=0.1mol,则含有氧原子的数目为0.1NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.常温下,已知0.1mol/L的CH3COOH和HCN溶液的pH分别为a、b,且1<a<b,下列有关叙述不正确的是( )
| A. | CH3COOH与HCN均为弱酸 | |
| B. | 常温下,等浓度CH3COONa溶液的pH小于NaCN溶液的pH | |
| C. | 在CH3COONa溶液中,c(Na+)+c(H+)═c(CH3COO-)+c(CH3COOH) | |
| D. | 在NaCN溶液中,c(Na+)>c(CN-) |
10.下列说法不正确的是( )
| A. | 盛有浓H2SO4 的烧杯在空气中敞口放置一段时间后,质量增加 | |
| B. | SO2 溶于水能导电,所以SO2 是电解质 | |
| C. | 标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内的氨水物质的量浓度为$\frac{1}{22.4}$ mol/L | |
| D. | 用蘸占有稀氨水的毛笔,在浸有酚酞溶液的滤纸上写出的字呈红色 |
7.下列关于Na2O2的说法中,不正确的是( )
| A. | 浅黄色固体 | B. | 可用作供氧剂 | ||
| C. | 与H2O反应时,H2O作还原剂 | D. | 与H2O反应时,放出热量 |
11.由钠、镁、铝、铁四种金属中的两种组成的混合物12克,与足量盐酸反应生成氢气0.5克,则该混合物的组成可能是( )
| A. | 钠和镁 | B. | 钠和铝 | C. | 钠和铁 | D. | 镁和铝 |
17.下列实验能达到实验目的且符合安全要求的是( )
| A. | 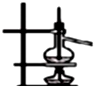 石油的蒸馏 | B. | 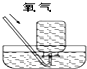 收集氧气 | ||
| C. | 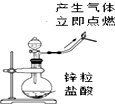 制备并检验氢气的可燃性 | D. | 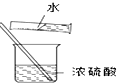 浓硫酸的稀释 |
18.下列说法正确的是( )
| A. | 纳米材料是指一种称为“纳米”的新物质制成的材料 | |
| B. | 光导纤维是以二氧化硅为主要原料制成的 | |
| C. | 玻璃在加热熔化时有固定的熔点 | |
| D. | 绿色食品是指不含任何化学物质的食品 |