ΧβΡΩΡΎ»ί
…ζΈο÷ Ρή «“Μ÷÷ΫύΨΜΓΔΩ…‘Ό…ζΡή‘¥ΓΘ…ζΈο÷ ΤχΘ®÷ς“Σ≥…Ζ÷ΈΣCOΓΔCO2ΓΔH2Β»Θ©”κΜλΚœΘ§‘ΎΚ§”–ZnΓΔCuΒ»‘ΣΥΊΒΡ¥ΏΜ·ΦΝΧθΦΰœ¬ΡήΚœ≥…“Μ÷÷…ζΈο÷ ΡήΓΣΓΣΦΉ¥ΦΓΘ
Θ®1Θ© ”κCOΜΞΈΣΒ»ΒγΉ”ΧεΒΡΈο÷ ΒΡΜ·―ß Ϋ « ΓΘ
Θ®2Θ© CO2Ζ÷Ή”÷–ΧΦ‘≠Ή”ΒΡ‘”Μ·άύ–Ά « ‘”Μ·ΓΘ
Θ®3Θ© Α¥ΒγΉ”≈≈≤ΦZn‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷– τ”Ύ «χΘ§
ΤδΨßΧε τ”ΎΝυΖΫΉνΟήΕ―ΜΐΘ§ΥϋΒΡ≈δΈΜ ΐ « ΓΘ
Θ®4Θ© CuΒΡ“Μ÷÷¬»Μ·ΈοΨßΧεΒΡΨßΑϊΫαΙΙ»γΆΦΥυ ΨΓΘΘ®Ω’–Ρ«ρ¥ζ±μ¬»άκΉ”Θ©Θ§‘ρ“ΜΗωΨßΑϊ÷–ΥυΚ§ΒΡ ΐΡΩ « ΓΘ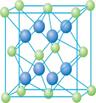
Θ®1Θ©N2Θ®2Θ©spΘ®3Θ©ds 12Θ®4Θ©4
ΫβΈω ‘ΧβΖ÷ΈωΘΚ Θ®1Θ©Β»ΒγΉ”Χε‘≠Ή” ΐœύΆ§ΓΔΦέΒγΉ” ΐœύΆ§ΓΘ”κCOΜΞΈΣΒ»ΒγΉ”ΧεΒΡΖ÷Ή” «N2ΓΘ
Θ®2Θ©CO2Ζ÷Ή”÷–CΦέ≤ψΒγΉ”Ε‘ ΐ= 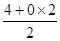 =2Θ§C‘”Μ·άύ–ΆΈΣspΓΘ
=2Θ§C‘”Μ·άύ–ΆΈΣspΓΘ
Θ®3Θ©–ΩΈΜ”ΎIIBΉεΘ§ τ”Ύds«χ‘ΣΥΊΓΘΝυΖΫΉνΟήΕ―Μΐ≈δΈΜ ΐΈΣ12ΓΘ
Θ®4Θ©ΨßΑϊ÷–¬Χ«ρΚΆάΕ«ρΗω ΐΖ÷±πΈΣ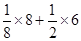 =4ΓΔ8ΓΘ
=4ΓΔ8ΓΘ
ΩΦΒψΘΚ Β»ΒγΉ”Χε ÷––Ρ‘≠Ή”‘”Μ·άύ–Ά ‘ΣΥΊ÷ήΤΎ±μΒΡΖ÷«χ Ϋπ τΨßΧεΕ―ΜΐΡΘ–Ά ΨßΑϊΦΤΥψ

œ¬±μ÷–ΥυΝ–ΒΡΉ÷ΡΗΖ÷±π¥ζ±μΡ≥“ΜΜ·―ß‘ΣΥΊΓΘΆξ≥…œ¬Ν–ΧνΩ’ΘΚ
| a | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | b | | |
| c | | | | | | | | | | | | d | | | e | f | |
| | | | | | | | | | | | | | g | | | | |
| | | | | | | | | | | | | | | | h | | |
| | i | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
Θ®1Θ©hΒΡΉνΆβ≤ψ”–____÷÷‘ΥΕ·Ή¥Χ§ΒΡΒγΉ”ΓΘaΓΔbΓΔc»ΐ÷÷‘ΣΥΊ–Έ≥…ΒΡΜ·ΚœΈοΒγΉ” ΫΈΣ________ΓΘ
Θ®2Θ©dΒΞ÷ »ή”ΎiΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡ»ή“Κ ±ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ____________ΓΘ
Θ®3Θ© ‘ΣΥΊe”κf‘ΣΥΊœύ±»Θ§Ζ«Ϋπ τ–‘Ϋœ«ΩΒΡ «__________Θ®–¥‘ΣΥΊΖϊΚ≈Θ©Θ§œ¬Ν–±μ ω÷–Ρή÷ΛΟς’β“Μ ¬ ΒΒΡ «__________Θ®―ΓΧν–ρΚ≈Θ©ΓΘ
a. eΒΡ“θάκΉ”ΜΙ‘≠–‘«Ω”ΎfΒΡ“θάκΉ” b. fΒΡ«βΜ·ΈοΥα–‘«Ω”ΎeΒΡ«βΜ·Έο
c. eΒΞ÷ ΒΡ»έΒψΗΏ”ΎfΒΞ÷ d. eΚΆf–Έ≥…ΒΡΜ·ΚœΈο÷–Θ§eœ‘’ΐΦέΘ§fœ‘ΗΚΦέ
Θ®4Θ©‘ΣΥΊXΘ®Ζ«aΓΪi‘ΣΥΊΘ© «Υυ‘Ύ÷ήΤΎ‘≠Ή”ΑκΨΕΉν¥σΒΡΖ«Ϋπ τ‘ΣΥΊΘ§ΥϋΒΡΤχΧ§«βΜ·ΈοΈΣ»ΐΫ«ΉΕ–ΈΦΪ–‘Ζ÷Ή”Θ§–¥≥ωX‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο_______________________________ΓΘ
XΓΔYΓΔZΓΔW «‘ΣΥΊ÷ήΤΎ±μ«ΑΥΡ÷ήΤΎ≥ΘΦϊΒΡΥΡ÷÷‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΓΘXΒΡΒΞ÷ Φ»”–Π“Φϋ¹V”–Π–ΦϋΘ§«“XΒΡΒΎ“ΜΒγάκΡή±»ΤδœύΝΎ‘ΣΥΊΕΦ¥σΘ§YΒΡΒγΗΚ–‘±»XΒΡ–ΓΘ§ΤδΜυΧ§‘≠Ή”ΉνΆβ≤ψΒΡpΒγΉ” «ΗΟ≤ψsΒγΉ”ΒΡΝΫ±ΕΘ§Z ««Α36Κ≈‘ΣΥΊ÷–‘≠Ή”ΑκΨΕΉν¥σΒΡ÷ςΉε‘ΣΥΊΘ§WΒΡ“Μ÷÷ΚΥΥΊΒΡ÷ ΝΩ ΐ «56Θ§÷–Ή” ΐ «30ΓΘ
(1) YΈΜ”Ύ‘ΣΥΊ÷ήΤΎ±μΒΎ_______÷ήΤΎΒΎ_______ΉεΘ§W2+ΒΡΚΥΆβΒγΉ”≈≈≤Φ Ϋ «______ΓΘ
(2) XΒΡ―θΜ·ΈοXO2”κH2O±»ΫœΘ§»έΒψΫœΗΏΒΡ «_______ (ΧνΜ·―ß Ϋ)Θ§ZΒΡ«βΜ·Έο τ”Ύ ΨßΧεΘ§Z2O2ΒΡΜ·―ßΦϋάύ–Ά «_______(Χν±ύΚ≈Θ©
| AΘ°άκΉ”Φϋ | BΘ°ΦΪ–‘Ι≤ΦέΦϋ | CΘ°Ζ«ΦΪ–‘Ι≤ΦέΦϋ | DΘ°Ϋπ τΦϋ |
(4)‘Ύ250CΘ§101kPaœ¬Θ§WΒΡΒΞ÷ ‘Ύ―θΤχ÷–»Φ…’ΚσΜ÷Η¥÷Ν‘≠Έ¬Ε»ΚΆ―Ι«ΩΘ§ΤΫΨυΟΩΉΣ“Τ1molΒγΉ”Ζ≈≥ωQkJΒΡ»»ΝΩΘ§‘ρWΒΞ÷ »Φ…’ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ «_______ΓΘ
XΓΪR «‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΕΧ÷ήΤΎ‘ΣΥΊΘ§Τδ–‘÷ ΜρΫαΙΙ–≈œΔ»γœ¬±μΘΚ
| ‘ΣΥΊ | X | Y | Z | W | R |
| –‘÷ –≈œΔ | Ρή–Έ≥…+7ΦέΒΡΜ·ΚœΈο | »’≥Θ…ζΜν÷–≥ΘΦϊΫπ τΘ§»έΜ· ±≤Δ≤ΜΒΈ¬δ,ΚΟœσ”–“Μ≤ψΡΛΕΒΉ≈ | Ά®≥ΘΉ¥Ωωœ¬Ρή–Έ≥…ΕΧ÷ήΤΎ÷–ΉνΈ»Ε®ΒΡΥΪ‘≠Ή”Ζ÷Ή” | ―φ…ΪΖ¥”ΠΈΣΜΤ…Ϊ | ΈΜ”ΎΒΎIVAΘ§ «–Έ≥…Μ·ΚœΈο÷÷άύΉνΕύΒΡ‘ΣΥΊ |
«κ”ΟΜ·―ß”Ο”οΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©X‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «_______ΓΘ
Θ®2Θ©‘ΣΥΊWΒΡάκΉ”ΫαΙΙ Ψ“βΆΦΈΣ_________ΓΘ
Θ®3Θ©‘ΣΥΊRΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΒγΉ” ΫΈΣ_________ΓΘ
Θ®4Θ©XΒΡ«βΜ·ΈοΚΆZΒΡ«βΜ·ΈοΖ¥”Π–Έ≥…Μ·ΚœΈοAΘ§A÷–Κ§”–ΒΡΜ·―ßΦϋάύ–ΆΈΣ_________Θ§ΫΪA »ή”ΎΥ°Θ§ΤδΥ°»ή“Κ÷–άκΉ”≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρ «_______________ ΓΘ
Θ®5Θ©Κ§YΒΡΡ≥Μ·ΚœΈοΩ…”ΟΉςΨΜΥ°ΦΝΘ§ΗΟΈο÷ ΒΡΥ°»ή“Κ≥ Υα–‘Θ§Τδ‘≠“ρ « ΓΘΘ®”ΟάκΉ”ΖΫ≥Χ Ϋ±μ ΨΘ©
Θ®6Θ©WΒΡ«β―θΜ·Έο «÷Ί“ΣΒΡΜυ±ΨΜ·ΙΛ‘≠ΝœΓΘ–¥≥ωΙΛ“Β…œ÷Τ»ΓΗΟ«β―θΜ·ΈοΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ Ϋ__________ ΓΘ
œ¬ΆΦΈΣ‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷Θ§ΗυΨί‘ΣΥΊΔΌΓΪΔύ‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷ΟΘ§Α¥“Σ«σΜΊ¥πœ¬Ν–Έ ΧβΓΘ
| Ήε ÷ήΤΎ | IA | | 0 | |||||
| 1 | ΔΌ | IIA | IIIA | ΔτA | VA | ΔωA | VIIA | |
| 2 | | | | | | ΔΎ | Δέ | |
| 3 | Δή | Δί | | | | Δό | ΔΏ | Δύ |
Θ®1Θ©‘Ύ‘ΣΥΊΔΌΓΪΔύ÷–Θ§Ϋπ τ–‘Ήν«ΩΒΡ‘ΣΥΊ «_____________Θ®Χν‘ΣΥΊΖϊΚ≈Θ©Θ§Ήν≤Μ»ί“Ή–Έ≥…Μ·ΚœΈοΒΡ‘ΣΥΊ «______________Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
Θ®2Θ©”ΟΒγΉ” Ϋ±μ ΨΔΏΒΡΤχΧ§«βΜ·ΈοΒΡ–Έ≥…Ιΐ≥Χ__________________________________ΓΘ
Θ®3Θ©ΔέΓΔΔήΓΔΔό÷–‘≠Ή”ΑκΨΕ”…¥σΒΫ–ΓΒΡΥ≥–ρ «____________________Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
Θ®4Θ©±μ÷–ΝΫ÷÷‘ΣΥΊΒΡ‘≠Ή”Α¥1ΘΚ1Ήι≥…ΒΡ≥ΘΦϊ“ΚΧ§Μ·ΚœΈοX“Ή±Μ¥ΏΜ·Ζ÷ΫβΓΘΡ≥Ά§―ß»Γ5÷ߥσ–ΓœύΆ§ΒΡ ‘ΙήΘ§ΗςΦ”»κΒ»Έο÷ ΒΡΝΩ≈®Ε»Β»ΧεΜΐΒΡX»ή“ΚΘ§Ζ÷±πΫχ––œ¬Ν– Β―ιΘ§―–ΨΩΆβΫγΧθΦΰΕ‘XΖ÷ΫβΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§ Β―ιΦ«¬Φ»γœ¬±μΥυ ΨΓΘ
| | –ρΚ≈ | ΧθΦΰ | œ÷œσ | Ϋα¬έ | |
| Έ¬Ε»Θ·Γφ | ¥ΏΜ·ΦΝ | ||||
| ΒΎ“ΜΉι | 1 | 40 | FeCl3»ή“Κ | ΩλΥΌ≤ζ…ζ¥σΝΩΤχ≈ί | œύΆ§ΧθΦΰœ¬Θ§Έ¬Ε»…ΐΗΏΘ§Μ·―ßΖ¥”ΠΥΌ¬ Φ”Ωλ |
| 2 | 20 | A | ΜΚ¬ΐ≤ζ…ζ ΝΩΤχ≈ί | ||
| 3 | 5 | FeCl3»ή“Κ | ΜΚ¬ΐ≤ζ…ζΦΪ…ΌΝΩΤχ≈ί | ||
| ΒΎΕΰΉι | 4 | t | MnO2 | ΩλΥΌ≤ζ…ζ¥σΝΩΤχ≈ί | |
| 5 | 20 | Έό | ΜΚ¬ΐ≤ζ…ζΦΪ…ΌΝΩΤχ≈ί | ||
ΔΌΒΎ“ΜΉι Β―ιΡΩΒΡ «ΘΚœύΆ§ΧθΦΰœ¬Θ§ΧΫΨΩ________________Ε‘ΗΟΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΓΘ
Β―ι2ΒΡ¥ΏΜ·ΦΝA «___________________ΓΘ
ΔΎΒΎΕΰΉι Β―ι÷–Θ§ Β―ι4ΒΡΈ¬Ε»t «_________________Θ§ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «___________________________________________________________________________ΓΘ
ΒΎΕΰΉι Β―ιΫα¬έ «ΘΚ__________________________________________________ΓΘ
œ¬±μ «‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷ΓΘ±μ÷–ΥυΝ–ΒΡΉ÷ΡΗΖ÷±π¥ζ±μ“Μ÷÷Μ·―ß‘ΣΥΊΓΘ
| | | | |||||||||||||||
| | | | | | a | | b | | |||||||||
| | | c | | | d | e | | ||||||||||
| | | | | | | | | f | | g | | | | | | | |
Θ®1Θ©aΒΡ«βΜ·ΈοΒΡΖ÷Ή”ΙΙ–ΆΈΣ Θ§÷––Ρ‘≠Ή”ΒΡ‘”Μ·–Έ ΫΈΣ ΘΜdΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΖ÷Ή”ΙΙ–ΆΈΣ Θ§÷––Ρ‘≠Ή”ΒΡ‘”Μ·–Έ ΫΈΣ Θ§ΗΟΖ÷Ή” « Θ®ΧνΓΑΦΪ–‘Γ±ΜρΓΑΖ«ΦΪ–‘Γ±Θ©Ζ÷Ή”ΓΘ
Θ®2Θ©bΓΔdΓΔe»ΐ÷÷‘ΣΥΊΒΡ«βΜ·Έο÷–ΒΡΖ–ΒψΉνΗΏΒΡ « Θ§‘≠“ρ «ΘΚ ΓΘ
Θ®3Θ©ΫΪgΒΡΈόΥ°ΝρΥα―Έ»ήΫβ”ΎΥ°÷–Θ§»ή“Κ≥ άΕ…ΪΘ§ «“ρΈΣ…ζ≥…ΝΥ“Μ÷÷≥ άΕ…ΪΒΡ≈δΚœάκΉ”Θ§–¥≥ωΗΟ≈δΚœάκΉ”ΒΡΫαΙΙΦρ Ϋ(±Ί–κΫΪ≈δΈΜΦϋ±μ Ψ≥ωά¥) ΓΘ
Θ®4Θ©f(NH3)5BrSO4Ω…–Έ≥…ΝΫ÷÷≈δΚœΈο Θ§“―÷Σf 3ΘΪ ΒΡ≈δΈΜ ΐ «6Θ§ΈΣ»ΖΕ®fΒΡ≈δΚœΈοΒΡΫαΙΙΘ§œ÷Ε‘ΝΫ÷÷≈δΚœΈοΫχ––»γœ¬ Β―ιΘΚ‘ΎΒΎ“Μ÷÷≈δΚœΈοΒΡ»ή“Κ÷–Φ”BaCl2»ή“Κ ±Θ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§‘ΎΒΎΕΰ÷÷≈δΚœΈο»ή“Κ÷–Φ”»κBaCl2»ή“Κ ±Θ§‘ρΈόΟςœ‘œ÷œσΘ§ΒΎΕΰ÷÷≈δΚœΈοΒΡΜ·―ß ΫΈΣ Θ§ΗΟ≈δΚœΈοΒΡ≈δΧε « ΓΔ ΘΜ
Θ®5Θ©cΒΞ÷ ΨßΧε÷–‘≠Ή”ΒΡΕ―ΜΐΖΫ Ϋ»γœ¬ΆΦΦΉΥυ ΨΘ§ΤδΨßΑϊΧΊ’ς»γœ¬ΆΦ““Υυ ΨΘ§‘≠Ή”÷°ΦδœύΜΞΈΜ÷ΟΙΊœΒΒΡΤΫΟφΆΦ»γœ¬ΆΦ±ϊΥυ ΨΓΘ
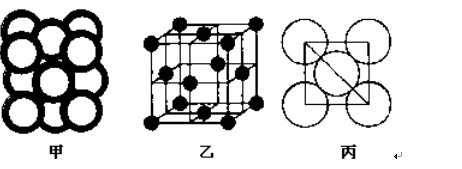
cΒΞ÷ ΨßΧε÷–‘≠Ή”ΒΡ≈δΈΜ ΐΈΣ ΓΘ»τ“―÷ΣcΒΡ‘≠Ή”ΑκΨΕΈΣrΘ§NA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΘ§cΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣMΓΘΗΟΨßΧεΒΡΟήΕ»ΈΣ Θ®”ΟΉ÷ΡΗ±μ ΨΘ©ΓΘ