题目内容
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如图:
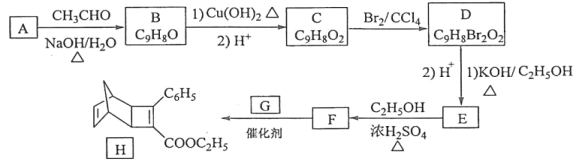
已知:
①RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
②![]()
回答下列问题:
(1)A的化学名称是___。
(2)由C生成D和E生成F的反应类型分别是__、__。
(3)E的结构简式为___。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为__。
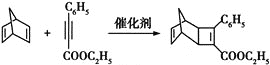
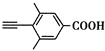
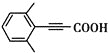
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出2种符合要求的X的结构简式__、__。
(6)写出用环戊烷和2–丁炔为原料制备化合物 的合成路线__(其他试剂任选)。
的合成路线__(其他试剂任选)。
【答案】苯甲醛 加成反应 取代反应 ![]()
 、
、
![]() 、
、
【解析】
芳香族化合物A与乙醛发生信息①中的反应生成B,A含有醛基,反应中脱去1分子水,由原子守恒可知A的分子式为:C9H8O+H2O-C2H4O=C7H6O,故A为![]() ,则B为
,则B为![]() ,B发生氧化反应、酸化得到C为
,B发生氧化反应、酸化得到C为![]() .C与溴发生加成反应得到D为
.C与溴发生加成反应得到D为![]() ,D发生消去反应、酸化得到E为
,D发生消去反应、酸化得到E为![]() .E与乙醇发生酯化反应生成F为
.E与乙醇发生酯化反应生成F为![]() ;结合信息②中的加成反应、H的结构简式,且G为甲苯的同分异构体,可推知G为
;结合信息②中的加成反应、H的结构简式,且G为甲苯的同分异构体,可推知G为![]() 。
。
(1)A为![]() ,其名称为苯甲醛;
,其名称为苯甲醛;
(2)C中碳碳双键和溴发生加成反应生成D,E和乙醇发生酯化反应(取代反应)生成F;
(3)根据分析可知E为![]() ;
;
(4)根据分析可知G为![]() ,F生成H的反应与信息②类似,所以化学方程式为
,F生成H的反应与信息②类似,所以化学方程式为![]() +
+![]()
![]()
 ;
;
(5)芳香化合物X是F(![]() )的同分异构体,X能饱和碳酸氢钠溶液反应放出CO2,说明含有羧基,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比之为6:2:1:1,说明分子结构对称,苯环上应有两个处于对位的取代基,符合要求的X的结构简式为:
)的同分异构体,X能饱和碳酸氢钠溶液反应放出CO2,说明含有羧基,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比之为6:2:1:1,说明分子结构对称,苯环上应有两个处于对位的取代基,符合要求的X的结构简式为: 、
、 、
、![]() 、
、 ;
;
(6)环戊烷为![]() ,2-丁炔为
,2-丁炔为![]() ,对比
,对比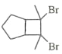 ,结合信息②,首先需要在五元环上生成双键,然后和2-丁炔反应,之后产物中的双键再与溴加成,烷基可以卤素单质发生取代反应,生成的卤代烃可以发生消去反应生成碳碳双键,所以合成路线为:
,结合信息②,首先需要在五元环上生成双键,然后和2-丁炔反应,之后产物中的双键再与溴加成,烷基可以卤素单质发生取代反应,生成的卤代烃可以发生消去反应生成碳碳双键,所以合成路线为: 。
。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】电镀行业产生的酸性含铬废水对环境有污染,其中所含的Cr(Ⅵ)是主要污染物,可采用多种处理方法将其除去。查阅资料可知:
①在酸性环境下,Cr(Ⅵ)通常以Cr2O72-的形式存在;
②Cr2O72-的氧化能力强于CrO42-;
③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
阳离子 | Fe3+ | Fe2+ | Cr3+ |
开始沉淀的pH | 1.9 | 7.0 | 4.3 |
沉淀完全的pH | 3.2 | 9.0 | 5.6 |
Ⅰ.腐蚀电池法
(1)向酸性含铬废水中投放废铁屑和焦炭,利用原电池原理还原Cr(Ⅵ)。下列关于焦炭的说法正确的是_______(填字母代号)。
a.作原电池的正极 b.在反应中作还原剂 c.表面可能有气泡产生
Ⅱ.电解还原法
向酸性含铬废水中加入适量NaCl固体,以Fe为电极电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准。电解装置如图1所示。
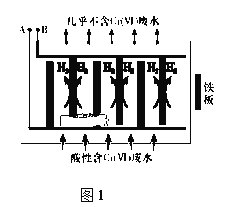
(2)A极连接电源的______________极,A极上发生的电极反应式为_______________
(3)电解开始时,B极上除了发生产生H2的反应外,还有少量Cr2O72-在B极上直接放电,该反应的电极反应式为_________________
(4)电解过程中,溶液的pH不同时,通电时间(t)与溶液中铬元素去除率的关系如图2所示。
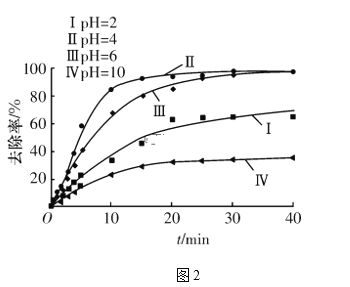
①由图可知,电解还原法应采取的最佳pH范围为____(填字母代号)。
a.2~4 b.4~6 c.6~10
②解释曲线Ⅰ和曲线Ⅳ去除率低的原因:________________
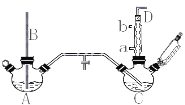
【题目】氯苯在染料、医药工业用于制造苯酚、硝基氯苯、苯胺、硝基酚等有机中间体,橡胶工业用于制造橡胶助剂。其合成工艺分为气相法和液相法两种,实验室模拟液相法(加热装置都已略去)如图,在C三颈烧瓶中加入催化剂FeCl3及50.0mL苯:
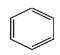 +Cl2
+Cl2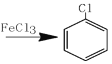 +HCl
+HCl
有关物质的性质:
名称 | 相对分子质量 | 沸点/(℃) | 密度/(g/mL) |
苯 | 78 | 78 | 0.88 |
氯苯 | 112.5 | 132.2 | 1.1 |
邻二氯苯 | 147 | 180.4 | 1.3 |
回答下列问题:
(1)A反应器是利用实验室法制取氯气,装置中空导管B的作用是__。
(2)把干燥的氯气通入装有干燥苯的反应器C中制备氯苯,C的反应温度不宜过高,原因为①温度过高,反应得到二氯苯;②__,球形冷凝管的作用是:__,D出口的主要尾气成分有__。
(3)提纯粗产品过程如图:

①净化过程中加入NaCl晶体的目的是吸水干燥,系列操作为__。
②为了确定所得产品为氯苯,而非二氯苯,可对产品进行分析,下列方法可行的是__。
A.质谱法 B.红外光谱法 C.滴定法
(4)实验中最终得到产品14.7g,产率为__,产率不高的原因可能是:___。
(5)苯气相氧氯化氢法制氯苯:空气、氯化氢气混合物温度210℃,进入氯化反应器,在迪肯型催化剂(CuCl2、FeCl3附在三氧化铝上)存在下进行氯化,反应方程式为:__。
【题目】某小组研究溶液中Fe2+与![]() 、
、![]() 的反应。
的反应。
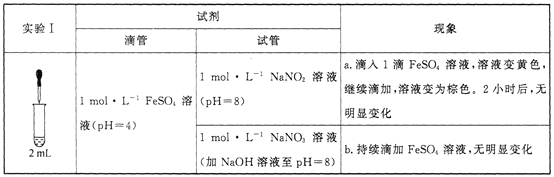
已知:[Fe(NO)]2+在溶液中呈棕色。
(1)研究现象a中的黄色溶液。
①用__________溶液检出溶液中含有Fe3+。
②甲认为是O2氧化了溶液中的Fe2+。乙认为O2不是主要原因,理由是_____________。
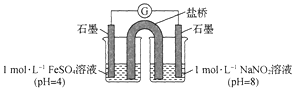
③进行实验Ⅱ,装置如图所示。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式为_______实验Ⅱ的目的是________。
(2)研究现象a中的棕色溶液。综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的Fe2+或Fe3+发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为Fe2+与NO发生了反应。实验Ⅲ的操作和现象是_______。
(3)研究酸性条件下,溶液中Fe2+与![]() 、
、![]() 的反应。
的反应。
序号 | 操作 | 现象 |
i | 取1 mol·L-l的NaNO2溶液,加稀硫酸至pH = 3,加入1 mol·L-l FeSO4溶液 | 溶液立即变为棕色 |
ii | 取1 mol·L-l的NaNO3溶液,加硫酸至pH = 3,加入1 mol·L-l FeSO4溶液 | 无明显变化 |
iii | 分别取0.5 mL l mol·L-l的NaNO3溶液与1 mol·L-l的FeSO4溶液,混合,小心加入0.5 mL浓硫酸 | 液体分为两层,稍后,在两层液体界面上出现棕色环 |
i中溶液变为棕色的离子方程式为_______、__________。
实验结论:本实验条件下,溶液中![]() 、
、![]() 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。