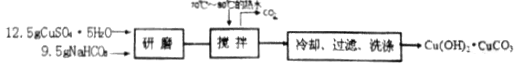
��Ŀ����
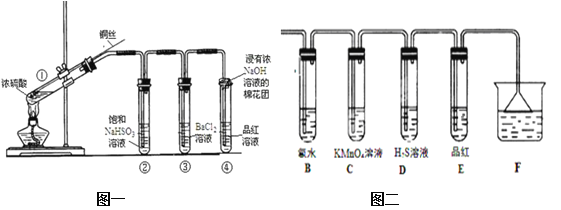
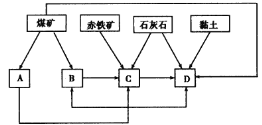
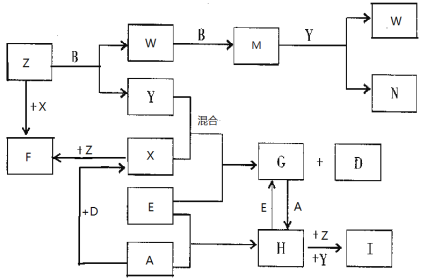
����Ŀ����֪A��B��C��D�Ƕ�����Ԫ�ص���̬���ʣ�����A�ǻ���ɫ�����嵥�ʣ�C�ڿ����к�����ߣ�D����������壻E��һ����õĽ�����Y��һ�ֳ�����Һ̬���ʣ�Z��Ψһ�Լ��Ե����壻 M��һ�ֺ���ɫ���ж����壻IΪ���ɫ������ˮ�Ĺ��塣�йص�ת����ϵ����ͼ��ʾ����Ӧ����������ȥ����
�ش��������⣺
��1��A�����Ԫ����Ԫ�����ڱ���λ��Ϊ ��
��2��F�л�ѧ���������� �� ����ÿ��2�֣���4�֣�
��3��Z��W�ڴ��������·�Ӧ����C��Y������һ������ʵ������ķ�Ӧ����������W�Ի�������Ⱦ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��4��IΪ���ɫ������ˮ�Ĺ��壬�롰84����Һ������Ч�ɷ�(NaClO) ����Ũ����Һ�з�����Ӧ�����˸�Ч�����ľ�ˮ���������ƣ���д���˷�Ӧ�����ӷ���ʽ ��
��5����������E�ӵ�N��ϡ��Һ�У���������ת�Ƶ��ӵ���ĿΪ3.01��1023����μӷ�Ӧ��E������Ϊ
g��
��������1���������ڵ�VIIA��
��2�����Ӽ���(����)���ۼ���
��3��4NH3��6NO![]() 5N2��6H2O��
5N2��6H2O��
��4��2Fe(OH)3 + 3ClO��+4OH��=2FeO42-+3Cl��+5H2O
��5��42
��������
�����������֪A��B��C��D�Ƕ�����Ԫ�ص���̬���ʣ�����A�ǻ���ɫ�����嵥�ʣ����A��������C�ڿ����к�����ߣ���C�ǵ�����D�����������������D���������������������������Ȼ��⣬��X���Ȼ��⡣E��һ����õĽ�������E�����������������������Ȼ�������H���Ȼ������Ȼ���������Ӧ�����Ȼ��������Ȼ�������������Ӧ�����Ȼ�������G���Ȼ�������Y��һ�ֳ�����Һ̬���ʣ���Y��ˮ���Ȼ�������ˮ�õ����ᣬ������Ӧ�����������Ȼ�������Z��Ψһ�Լ��Ե���������Z�ǰ�����������ˮ�Լ��Ȼ�����Ӧ��������������������I������������Ϊ���ɫ������ˮ�Ĺ������������Ȼ��ⷴӦ�����Ȼ�泥���F���Ȼ�李�M��һ�ֺ���ɫ���ж���������M��NO2��������B��Ӧ����ˮ��W��W��B��Ӧ���ɶ�����������˵��B��������W��NO��������������ˮ�õ�NO�����ᣬ��N�����ᡣ
��1��A�����Ԫ������Ԫ�أ���Ԫ�����ڱ���λ��Ϊ�������ڵ�VIIA����
��2��F���Ȼ�泥����л�ѧ�������������Ӽ����ۼ���
��3��Z��W�ڴ��������·�Ӧ����������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ4NH3��6NO![]() 5N2��6H2O��
5N2��6H2O��
��4�����������롰84����Һ������Ч�ɷ�(NaClO) ����Ũ����Һ�з�����Ӧ�����˸�Ч�����ľ�ˮ���������ƣ��˷�Ӧ�����ӷ���ʽΪ2Fe(OH)3 + 3ClO��+4OH��=2FeO42-+3Cl��+5H2O��
��5�������������ӵ�������ϡ��Һ����������������NO��ˮ����������ת�Ƶ��ӵ���ĿΪ3.01��1023������ʧȥ�ĵ��ӵ����ʵ�����0.5mol�����Բμӷ�Ӧ������0.25mol�������������������0.25mol�����ݵ��ӵ�ʧ�غ��֪����NO��0.5mol��3�����Ը��ݵ�ԭ���غ��֪�μӷ�Ӧ��E������Ϊ��0.25mol��2��0.5mol��3����63g/mol��42g��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�