题目内容
【题目】某研究性学习小组以甲酸为原料在实验室完成了一氧化碳和甲酸铜两种物质的制备实验。
实验一、用甲酸制备一氧化碳
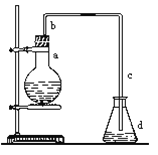
CO的制备原理:HCOOH![]() CO↑+H2O,制备装置如下图(其中夹持仪器、加热仪器没有画出)
CO↑+H2O,制备装置如下图(其中夹持仪器、加热仪器没有画出)
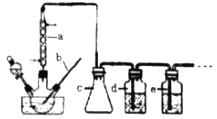
(1)b仪器的名称为___________,c的作用是___________。
(2)制备CO时,浓硫酸与甲酸的混合方式是___________。
实验二、用甲酸制备甲酸铜[Cu(HCOO)24H2O]
步骤一:碱式碳酸铜的制备
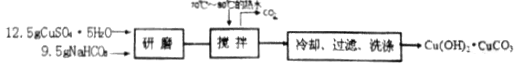
步骤二:甲酸铜的制备
将产品碱式碳酸铜放入烧杯内,加入约20mL蒸馏水,加热搅拌至323K左右,逐滴加入适量甲酸至沉淀完全溶解,趁热过滤,滤液在通风橱下蒸发至原体积的![]() 左右,冷却至室温,减压过滤,洗涤,得Cu(HCOO)24H2O产品,称量,计算产率。回答下列问题:
左右,冷却至室温,减压过滤,洗涤,得Cu(HCOO)24H2O产品,称量,计算产率。回答下列问题:
(3)在制备碱式碳酸铜的过程中,如果温度过高,对产物有何影响?___________。
(4)步骤二中碱式碳酸铜滴入甲酸生成四水合甲酸铜的化学方程式为___________。
(5)本实验涉及三种固液分离的方法.
①倾析法使用到的仪器有___________;
②采用减压过滤的装置对步骤二中溶解后的溶液进行趁热过滤;
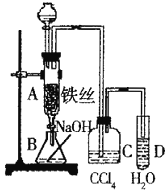
③步骤二的实验中,需用到下列装置___________

(6)最终称量所得的产品为7.91g,则产率为___________。
【答案】
(1)温度计;防倒吸
(2)先加热浓硫酸至80℃-90℃,再逐滴滴入甲酸
(3)温度过高导致Cu(OH)2CuCO3分解;
(4)Cu(OH)2CuCO3+4HCOOH+5H2O═Cu(HCOO)24H2O+CO2↑
(5)①烧杯、玻璃棒;③ CDF
(6)70﹪
【解析】
试题分析:(1)根据装置图,b仪器是温度计,c是安全瓶,可以防止倒吸,故答案为:温度计;防倒吸
(2)反应中浓硫酸主要起催化剂和脱水剂的作用,,反应时首先加热浓硫酸至80℃-90℃,再逐滴滴入甲酸,就会反应放出一氧化碳,故答案为:先加热浓硫酸至80℃-90℃,再逐滴滴入甲酸;
(3)用于碱式碳酸铜不稳定,温度过高导致Cu(OH)2CuCO3分解生成黑色的氧化铜、二氧化碳气体和水,影响其产率,故答案为:温度过高导致Cu(OH)2CuCO3分解;
(4)碱式碳酸铜与甲酸反应制得蓝色四水甲酸铜的反应方程式为Cu(OH)2CuCO3+4HCOOH+5H2O═Cu(HCOO)24H2O+CO2↑,故答案为:Cu(OH)2CuCO3+4HCOOH+5H2O═Cu(HCOO)24H2O+CO2↑;
(5)①倾析法分离溶液时,选用使用到烧杯和用于引流的仪器玻璃棒,故答案为:烧杯、玻璃棒;
③根据甲酸铜的制备步骤可知,需要减压过滤、趁热过滤和蒸发装置,所以需要的装置有C、D、F,故答案为:CDF;
(6)12.5g硫酸铜晶体的物质的量为:![]() =0.05mol,9.5g碳酸氢钠的物质的量为:
=0.05mol,9.5g碳酸氢钠的物质的量为:![]() ≈0.113mol,根据反应2CuSO4+4NaHCO3═Cu(OH)2CuCO3↓+3CO2↑+2Na2SO4+H2O可知,碳酸氢钠过量,反应生成的碱式碳酸铜的物质的量为0.05mol,根据反应Cu(OH)2CuCO3+4HCOOH+5H2O═Cu(HCOO)24H2O+CO2↑可知,生成甲酸铜的物质的量为0.05mol,所以甲酸铜的产率为:
≈0.113mol,根据反应2CuSO4+4NaHCO3═Cu(OH)2CuCO3↓+3CO2↑+2Na2SO4+H2O可知,碳酸氢钠过量,反应生成的碱式碳酸铜的物质的量为0.05mol,根据反应Cu(OH)2CuCO3+4HCOOH+5H2O═Cu(HCOO)24H2O+CO2↑可知,生成甲酸铜的物质的量为0.05mol,所以甲酸铜的产率为:![]() ×100%=70%,故答案为:70%。
×100%=70%,故答案为:70%。

【题目】短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 和E同主族 |
C | lmo1C单质能与冷水反应,在标准状况下生成11.2LH2 |
D | 原子最外层电子数等于其周期序数 |
E | 负一价阴离子的电子层结构与Ar原子相同 |
(1) A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
A.比较两种单质的颜色
B.比较两种单质与H2化合的难易程度
C.依据两元素在周期表中的位置
D.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。