题目内容
【题目】氮的氧化物处理和利用是环境科学研究的热点。
Ⅰ.碱吸法。用烧碱溶液吸收NO、NO2制备亚硝酸盐:2NaOH+NO2+NO=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O。已知:298K时,Ka(HNO2)=5×10-4。
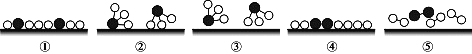
(1)298K时,NaNO2的水解常数约为______________。
Ⅱ.电解法。工业上以石墨为电极,用硝酸铵稀溶液作电解质溶液电解NO获得氮肥(在电解后溶液中通入适量氨气),其原理为8NO+7H2O+2NH3![]() 5NH4NO3。
5NH4NO3。
(2)阴极的电极反应式为_______________。
(3)阳极区电解质溶液的pH________(填“增大”“减小”或“不变”)。
Ⅲ.化合法。亚硝酸酰氯(NOCl)是有机合成中的重要试剂,可用NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)![]() 2NOCl(g)。
2NOCl(g)。
(4)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
热化学方程式 | 平衡常数 | |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
△H1、△H2、△H3之间的关系为_____________;K3=________(用含K1、K2的关系式表示)。
(5)在2L恒容容器中充入4molNO(g)和2molCl2(g),在不同温度下测得c(NOCl)与时间(t)的关系如图所示。
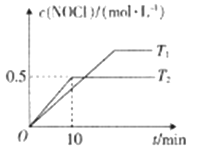
①T2时反应0~10min内NOCl的平均反应速率v(NOCl)=______mol·L-1·min-1。
②T2时反应的平衡常数K为__________;NO的平衡转化率α(NO)为_________。
③T2时向上述平衡体系中再加入1molNO(g)、1molCl2(g)、2molNOCl(g),则平衡______(填“向左”“向右”或“不”)移动。
(6)在密闭容器中充入NO(g)和Cl2(g),改变外界条件,Cl2的转化率变化如图所示。则该条件可能为____(填字母)。
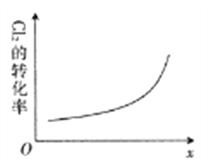
A.升高温度 B.增大压强 C.增大起始投料比![]() D.增大催化剂接触面
D.增大催化剂接触面
【答案】 2.0×10-11 NO+6H++5e-=NH4++H2O 减小 △H3=2△H1-△H2 K3=K12/K2 0.05 1/6.75 25% 向左 B
【解析】已知:298K时,Ka(HNO2)=5×10-4。
(1)298K时,NaNO2的水解的离子方程式为NO2-+H2O ![]() HNO2+OH-常数约为
HNO2+OH-常数约为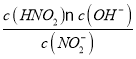 =
=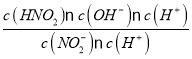 =
= ![]()
![]() Kw =
Kw = ![]()
![]() =2.0×10-11
=2.0×10-11
(2)阴极发生还原反应,电极反应式为NO+6H++5e-=NH4++H2O .
(3)阳极发生氧化反应,水电离的氢氧根放电,电极反应式为2H2O-4e-=O2↑+4H+,所以电解质溶液的pH减小。
(4)分析表中三个反应之间的关系,发现③=①![]() 2-②,所以△H1、△H2、△H3之间的关系为△H3=2△H1-△H2 ;
2-②,所以△H1、△H2、△H3之间的关系为△H3=2△H1-△H2 ;
K3= =
= 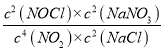
![]()
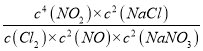 =K12/K2 。
=K12/K2 。
(5)在2L恒容容器中充入4molNO(g)和2molCl2(g):
2NO(g)+ Cl2(g) ![]() 2NOCl(g)
2NOCl(g)
起始量(mol/L) 2 1 0
T2变化量(mol/L) 0.5 0.25 0.5
T2平衡量(mol/L) 1.5 0.75 0.5
①T2时反应0~10min内NOCl的平均反应速率
v(NOCl)= ![]() = 0.05mol·L-1·min-1。
= 0.05mol·L-1·min-1。
②T2时反应的平衡常数K=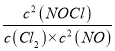 =
= ![]() = 1/6.75;NO的平衡转化率α(NO)=
= 1/6.75;NO的平衡转化率α(NO)= ![]()
![]() 100%=25%。
100%=25%。
③T2时向上述平衡体系中再加入1molNO(g)、1molCl2(g)、2molNOCl(g),求出此时Qc=![]() span> =0.45>1/6.75,所以则平衡向左移动。
span> =0.45>1/6.75,所以则平衡向左移动。
(6)由上面图像可知,T2先达平衡,所以T2>T1,升高温度后生成物NOCl的平衡浓度减小,所以正反应是气体体积减小的放热反应。在密闭容器中充入NO(g)和Cl2(g),改变外界条件,Cl2的转化率随横坐标的增大而增大,说明改变的条件有利于正反应的发生,这个条件只能选B增大压强。因为升高温度平衡向逆反应方向移动,C增大投料比,氯气的转化率将减小,D增大催化剂的接触面能同等程度增大正、逆反应的速率,但是平衡不发生移动。

【题目】(10分)研究有机物一般经过以下几个基本步骤:分离、提纯 → 确定实验式 → 确定分子式 → 确定结构式。
已知:① 2R-COOH + 2Na → 2R-COONa + H2↑
② R-COOH + NaHCO3→ R-COONa + CO2↑ + H2O
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实 验 步 骤 | 解 释 或 实 验 结 论 |
(1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: |
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
|
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 | (3)用结构简式表示A中含有的官能团 |
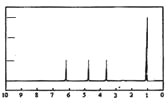
(4)A的核磁共振氢谱如下图: |
|