题目内容
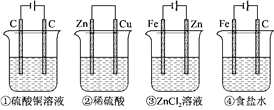
【题目】如图,四种装置中所盛的溶液体积均为500mL,浓度均为0.6molL-1,(③可以实现铁表面镀锌)工作一段时间后,测得导线上均通过了0.2mol电子,此时溶液中的pH由大到小的顺序是
A. ④②①③
B. ④③①②
C. ④③②①
D. ①③②④
【答案】B
【解析】根据装置可知,①是电解硫酸铜溶液的,根据反应式2CuSO4+2H2O2![]() Cu+2H2SO4+O2↑可知,溶液中生成0.2mol氢离子;②是原电池,消耗0.2mol氢离子,剩余氢离子
Cu+2H2SO4+O2↑可知,溶液中生成0.2mol氢离子;②是原电池,消耗0.2mol氢离子,剩余氢离子![]() =0.1mol;③是铁上镀锌,溶液的pH不变;④是电解饱和食盐水,根据反应式2Cl-+2H2O
=0.1mol;③是铁上镀锌,溶液的pH不变;④是电解饱和食盐水,根据反应式2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑可知,溶液中生成0.2molOH-,所以溶液中的pH由大到小的顺序是④③①②,答案选B。
2OH-+H2↑+Cl2↑可知,溶液中生成0.2molOH-,所以溶液中的pH由大到小的顺序是④③①②,答案选B。

练习册系列答案
相关题目